某氣體物質的質量為6.4g,含有6.02×1022個分子,則該氣體的相對分子質量是( )
A.64
B.32
C.96
D.124
【答案】
分析:根據n=
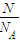
計算該氣體的物質的量,再根據M=
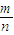
計算該氣體的摩爾質量,當摩爾質量以g/mol作單位,數值上等于其相對分子質量.
解答:解:6.4g該氣體的物質的量為
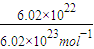
=0.1mol.
該氣體的摩爾質量為
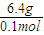
=64g/mol,
當摩爾質量以g/mol作單位,數值上等于其相對分子質量,所以該氣體的相對分子質量為64.
故選:A.
點評:考查相對分子質量的計算,比較基礎,掌握相對分子質量的計算方法.
