
【題目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成兩份。向其中一份中逐漸加入銅粉,最多能溶解9.6 g。向另一份中逐漸加入鐵粉,產生氣體的量隨鐵粉質量增加的變化如下圖所示(已知硝酸只被還原為NO氣體),下列分析或結果錯誤的是

A. 原混合酸中HNO3的物質的量為0.1 mol
B. OA段產生的是NO,AB段的反應為Fe+2Fe3+ == 3Fe2+,BC段產生氫氣
C. 第二份溶液中最終溶質為FeSO4
D. H2SO4濃度為2.5 mol·L-1
【答案】A
【解析】試題分析:由圖像可知,OA段發生反應為:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段發生反應為:Fe+2Fe3+=3Fe2+,BC段發生反應為:Fe+2H+=Fe2++H2↑。A.OA段發生反應為:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化劑作用,所以n(NO3-)=n(Fe)=5.6g÷56g/mol=0.1mol,因為溶液分為兩部分,所以原來溶液中n(NO3-)=0.1mol×2=0.2mol,A錯誤; B、由圖像可知,由于鐵過量,OA段發生反應為:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段發生反應為:Fe+2Fe3+=3Fe2+,BC段發生反應為:Fe+2H+=Fe2++H2↑,故B正確;C、硝酸全部被還原,沒有顯酸性的硝酸,因為溶液中有硫酸根,并且鐵單質全部轉化為亞鐵離子,所以溶液中最終溶質為FeSO4,C正確;D、反應消耗14g鐵,即0.25mol鐵,所有的鐵都在硫酸亞鐵中,根據硫酸根守恒,所以每份含硫酸0.4mol,所以硫酸的濃度是0.25mol÷0.1L==2.5mol/L,D正確;答案選A。


 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式中,正確的是( )
A.氯水與足量的 FeBr2溶液反應:2Fe2++4Br﹣+3Cl2=2Fe3++2Br2+6Cl﹣
B.NaHCO3溶液與 NaOH溶液反應:HCO ![]() +OH﹣=CO
+OH﹣=CO ![]() +H2O
+H2O
C.NaHCO3溶液與鹽酸反應:CO ![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
D.NaHCO3溶液與CaCl2;溶液反應:CO ![]() +Ca2+=CaCO3↓
+Ca2+=CaCO3↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用相關知識填空:
(1)在標準狀況下,下列物質:①4gH2、②11.2LO2、③1molH2O中,所含分子數最多的是 , (填序號,下同),含原子數最多的是 , 質量最大的是 , 體積最小的是 .
(2)在一定的溫度和壓強下,1體積X2(氣)跟3體積Y2(氣)化合生成2體積化合物,則該化合物的化學式是;
(3)19g某二價金屬的氯化物ACl2中含有0.4molCl﹣離子,ACl2的相對分子質量是 , A2+的摩爾質量為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干種,取該溶液進行連續實驗,實驗過程如下(所加試劑均過量,氣體全部逸出)下列說法不正確的是:
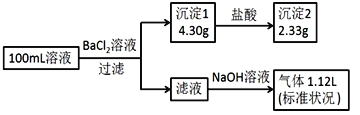
A. 原溶液一定存在CO32-、SO42-、NH4+
B. 原溶液一定存在Cl-,一定不存在Fe3+
C. 可能存在Na+,可以通過焰色反應證明其是否存在
D. 若原溶液中不存在Na+,則c(Cl-)<0.1mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在一個2 L的密閉容器中加入4 mol A和2 mol B進行如下反應:3A(g)+2B(g)![]() 4C(s)+D(g),反應2 min后達到平衡,測得生成1.6 mol C,下列說法正確的是
4C(s)+D(g),反應2 min后達到平衡,測得生成1.6 mol C,下列說法正確的是
A. 前2 min,D的平均反應速率為0.2 mol·L-1·min-1 B. 此時,B的平衡轉化率是40%
C. 升高該體系的溫度,化學平衡常數不變 D. 增加C,逆向速率增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國“長征二號F”運載火箭發射現場.可以看到從火箭的下部噴射出大量的紅棕色的氣體,關于這種紅棕色氣體的認識正確的是
A.是溴蒸氣,火箭發射時作氧化劑
B.是二氧化氮氣體,火箭發射時作還原劑
C.是溴蒸氣,火箭發射時作還原劑
D.是二氧化氮氣體,火箭發射時作氧化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)室溫下,0.1 mol/L的下列溶液中,①NH4Al(SO4)2 ②NH4HSO4 ③HCl ④(NH4)2SO4 ⑤NH4Cl ⑥NH4HCO3 ,pH由大到小的順序為__________(填寫序號)
(2)加熱,逐漸蒸干FeSO4溶液,得到的物質為___________。(填化學式)
(3)如圖是0.1 mol/L電解質溶液的pH隨溫度變化的圖象。

①其中符合0.1 mol/L NH4Al(SO4)2溶液的pH隨溫度變化的曲線是_____(填寫羅馬數字)
②25 ℃時,0.1 mol/L的NH4Al(SO4)2溶液中2c(![]() )-c(
)-c(![]() )-3c(Al3+)=____(填數值)。
)-3c(Al3+)=____(填數值)。
(4)室溫時,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH與所加NaOH溶液體積的關系曲線如圖所示:

試分析圖中a、b、c、d四個點,水的電離程度最大的是____;在b點,溶液中各離子濃度由大到小的排列順序是______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】液氨氣化后,分解產生的氫氣可作為氫氧燃料電池的燃料。氨氣分解反應的熱化學方程式如下:2NH3(g) ![]() N2 (g) + 3H2(g) ΔH = + a kJ·mol-1 (a>0)。請回答下列問題:
N2 (g) + 3H2(g) ΔH = + a kJ·mol-1 (a>0)。請回答下列問題:
已知:2H2 (g) + O2 (g) =2H2O(l) ΔH1 = - b kJ·mol-1
NH3 (g) ![]() NH3(l) ΔH2 = - c kJ·mol-1
NH3(l) ΔH2 = - c kJ·mol-1
(1)氨氣自發分解的反應條件為________(填“高溫”、“ 低溫”、“ 任何條件下”),4NH3(l) + 3O2 (g) = 2N2 (g) + 6H2O(l) 的 ΔH3 =_____________kJ·mol-1。
(2)H2O的電子式為_____________,水能發生電離:2H2O(l) ![]() H3O++OH-,液氨也能發生類似的電離。請寫出液氨的電離方程式____________________________________。
H3O++OH-,液氨也能發生類似的電離。請寫出液氨的電離方程式____________________________________。
(3)液氨氣化后,分解產生的氫氣可作為氫氧燃料電池的燃料,在KOH電解質溶液中,電池負極的電極反應為__________________________________________,實驗室中用氫氧燃料電池作為電源采用Pt電極對液氨進行電解可以得到H2和N2 ,若電解過程中陽極收集得到4.48L氣體(標況),則轉移的電子的數目是_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的質量(m)和通入CO2體積(V)的關系如圖所示: 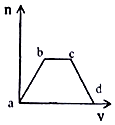
(1)ab段發生的離子反應方程式為 .
(2)bc段依次發生兩個離子反應,首先是 , 其次是 .
(3)cd段發生的離子反應方程式是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com