
【題目】為探究工業尾氣處理副產品X(黑色固體,僅含兩種元素)的組成和性質,設計并完成如下實驗:

請回答:
(1)X含有的兩種元素是__________,其化學式是____________。
(2)無色氣體D與氯化鐵溶液反應的離子方程式是____________________。
(3)已知化合物X能與稀鹽酸反應,生成一種淡黃色不溶物和一種氣體(標況下的密度為1.518 g·L-1),寫出該反應的化學方程式________________________________________。
【答案】Fe、S Fe2S3 SO2 + 2Fe3+ + 2H2O = 2Fe2+ + SO42- + 4H+ Fe2S3 + 4HCl = 2H2S↑+ 2FeCl2 + S↓
【解析】
本題考查化學反應流程圖、離子反應方程式的書寫及物質的推斷等知識。根據向B加入KSCN溶液后,C為血紅色溶液為突破口,可以推知B為FeCl3,C為Fe(SCN)3,可知A為Fe2O3,且n(Fe2O3) = 32g/160g/mol = 0.2 mol,n(Fe) = 0.4 mol,m(Fe) = 0.4mol![]() 56g/mol = 22.4g,X燃燒生成的無色氣體D,D使FeCl3溶液變為淺綠色,再加BaCl2生成白色沉淀,可知含有X中含有S元素。再根據各元素的質量求出個數比,據此分析作答。
56g/mol = 22.4g,X燃燒生成的無色氣體D,D使FeCl3溶液變為淺綠色,再加BaCl2生成白色沉淀,可知含有X中含有S元素。再根據各元素的質量求出個數比,據此分析作答。
(1)B加入KSCN,C為血紅色溶液,可以知道B為FeCl3,C為Fe(SCN)3等,可知A為Fe2O3,且n(Fe2O3) = 32g/160g/mol = 0.2 mol,n(Fe) = 0.4 mol,m(Fe) = 0.4mol![]() 56g/mol = 22.4g,X燃燒生成的無色氣體D,D使FeCl3溶液變為淺綠色,再加BaCl2生成白色沉淀,可知含有X中含有S元素,且m(S) = 41.6g-22.4g = 19.2g,n(S)=
56g/mol = 22.4g,X燃燒生成的無色氣體D,D使FeCl3溶液變為淺綠色,再加BaCl2生成白色沉淀,可知含有X中含有S元素,且m(S) = 41.6g-22.4g = 19.2g,n(S)= ![]() = 0.6mol,可以知道n(Fe):n(S) = 2:3,應為Fe2S3,故答案為:Fe、S;Fe2S3;
= 0.6mol,可以知道n(Fe):n(S) = 2:3,應為Fe2S3,故答案為:Fe、S;Fe2S3;
(2)無色氣體D為SO2,與氯化鐵發生氧化還原反應,離子方程式為SO2 + 2Fe3+ + 2H2O = 2Fe2+ + SO42- + 4H+,故答案為:SO2 + 2Fe3+ + 2H2O = 2Fe2+ + SO42- + 4H+;
(3)化合物X能與稀硫酸反應,生成一種淡黃色不溶物和一種氣體(標況下的密度為1.518g/L,淡黃色不溶物為S,氣體的相對分子質量為1.518×22.4L=34,為H2S氣體,該反應的化學方程式為Fe2S3 + 4HCl = 2H2S↑+ 2FeCl2 + S↓,故答案為:Fe2S3 + 4HCl = 2H2S↑+ 2FeCl2 + S↓


科目:高中化學 來源: 題型:
【題目】下列實驗操作可達到實驗目的的是
A. 用長頸漏斗可分離乙酸乙酯和飽和碳酸鈉溶液
B. 將NaOH溶液滴加到FeCl3溶液中可制備Fe(OH)3膠體
C. 用濃鹽酸和MnO2反應制備純凈的Cl2,氣體產物先通過濃硫酸再通過飽和食鹽水
D. 除去Na2CO3固體中的NaHCO3,可將固體加熱至恒重
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從工業廢釩中回收金屬釩既避免污染環境又有利于資源綜合利用。某工業廢釩的主要成分為V2O5、VOSO4和SiO2等,下圖是從廢釩中回收釩的一種工藝流程:

(1)為了提高“酸浸”效率,可以采取的措施有________(填兩種).
(2)“還原”工序中反應的離子方程式為________.
(3)“沉釩”得到NH4VO3沉淀,需對沉淀進行洗滌,檢驗沉淀完全洗凈的方法是________.
(4)寫出流程中鋁熱反應的化學方程式________.
(5)電解精煉時,以熔融NaCl、CaCl2和VCl2為電解液(其中VCl2以分子形式存在).粗釩應與電源的________極(填“正”或“負”)相連,陰極的電極反應式為________.
(6)為預估“還原”工序加入H2C2O4的量,需測定“酸浸”液中VO2+的濃度.每次取25.00mL“酸浸”液于錐形瓶用a mol/L(NH4)2Fe(SO4)2標準溶液和苯代鄰氨基苯甲酸為指示劑進行滴定(其中VO2+ VO2+),若三次滴定消耗標準液的體積平均為bmL,則VO2+的濃度為________g/L(用含a、b的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組進行實驗:向硫酸酸化的過氧化氫溶液中加入碘化鉀、淀粉和硫代硫酸鈉的混合溶液,一段時間后溶液變藍。查閱資料知體系中存在兩個主要反應:
反應i:H2O2(aq) + 2I-(aq) + 2H+(aq) I2(aq) + 2H2O(l) ΔH1 = -247.5 kJ/mol
反應ii:I2(aq) + 2S2O32-(aq) 2I-(aq) + S4O62-(aq) ΔH2 = -1021.6 kJ/mol
(1)H2O2與S2O32-反應的熱化學方程式為______。
(2)下列實驗方案可證實上述反應過程。將實驗方案補充完整(所用試劑濃度均為0.01 mol/L)。
a.向酸化的H2O2溶液中加入________溶液,溶液幾秒后變為藍色。
b._________,溶液立即褪色。
(3)探究c(H+)對反應速率的影響,實驗方案如下表所示。(所用試劑除H2O以外,濃度均為0.01 mol/L)
實驗序號 | a | b | |
試 劑 | H2O2/mL | 5 | ______ |
H2SO4/mL | 4 | 2 | |
Na2S2O3/mL | 8 | _____ | |
KI(含淀粉)/mL | 3 | _____ | |
H2O | 0 | ______ | |
將上述溶液迅速混合 觀察現象 | 溶液變藍所需時間 為t1秒 | 溶液變藍所需時間 為t2秒 | |
① 將實驗b補充完整。
② 對比實驗a和實驗b,t1_____t2(填“>”或“<”)。
③ 結合(2)中現象解釋溶液混合后一段時間才變藍的原因________。
④ 利用實驗a的數據,計算t1時間內H2O2與S2O32-反應的平均反應速率(用H2O2濃度的變化表示)________mol/(L·s)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒溫、體積為1.0L的密閉容器中通入1.0 mol N2和x mol H2發生如下反應N2(g)+3H2(g)![]() 2NH3(g),20 min后達到平衡,測得反應放出的熱量為18.4 kJ,混合氣體的物質的量為1.6 mol,容器內的壓強變為原來的80%。請回答下列問題:
2NH3(g),20 min后達到平衡,測得反應放出的熱量為18.4 kJ,混合氣體的物質的量為1.6 mol,容器內的壓強變為原來的80%。請回答下列問題:
(1)20 min內,υ(N2)=____________________。
(2)該反應的熱化學方程式為______________________________。
(3)下列敘述中能表示該反應達到平衡狀態的是_________(填序號)。
①N2體積分數保持不變
②單位時間斷裂0.3 mol H-H鍵,同時生成0.6 mol N-H鍵
③混合氣體的密度不再改變
④2υ正(H2)=3υ逆(NH3)
⑤混合氣體的平均摩爾質量不再改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】MgCO3和CaCO3的能量關系如圖所示(M=Ca、Mg):
M2+(g)+CO32-(g) ![]() M2+(g)+O2(g)+CO2(g)
M2+(g)+O2(g)+CO2(g)
![]()
![]()
![]()
已知:離子電荷相同時,半徑越小,離子鍵越強。下列說法不正確的是
A. ΔH1(MgCO3)>ΔH1(CaCO3)>0
B. ΔH2(MgCO3)=ΔH2(CaCO3)>0
C. ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO)
D. 對于MgCO3和CaCO3,ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,C和水在密閉容器中發生下列反應:C(s)+H2O(g)![]() CO(g)+H2(g),CO(g)+H2O(g)
CO(g)+H2(g),CO(g)+H2O(g)![]() CO2(g)+H2(g)當反應達平衡時,測得c(H2)=1.9 mol/L,c(CO)=0.1 mol/L,則CO2的濃度為
CO2(g)+H2(g)當反應達平衡時,測得c(H2)=1.9 mol/L,c(CO)=0.1 mol/L,則CO2的濃度為
A. 0.1 mol/L B. 0.9 mol/L C. 1.8 mol/L D. 1.9 mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組擬合成除草劑苯達松和染料中間體X。
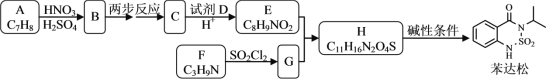
已知信息:①![]() +RCOOR′
+RCOOR′![]()
![]()
②RCH2COOR′+R′′COOR′′′![]()
![]()
(1)下列說法正確的是________。
A.化合物B到C的轉變涉及到取代反應
B.化合物C具有兩性
C.試劑D可以是甲醇
D.苯達松的分子式是C10H10N2O3S
(2)化合物F的結構簡式是________。
(3)寫出E+G→H的化學方程式________。
(4)寫出C6H13NO2同時符合下列條件的同分異構體的結構簡式________。
①分子中有一個六元環,且成環原子中最多含2個非碳原子;
②1HNMR譜和IR譜檢測表明分子中有4種化學環境不同的氫原子。有N-O鍵,沒有過氧鍵(-O-O-)。
(5)設計以CH3CH2OH和 原料制備X(
原料制備X( )的合成路線(無機試劑任選,合成中須用到上述①②兩條已知信息,用流程圖表示)________。
)的合成路線(無機試劑任選,合成中須用到上述①②兩條已知信息,用流程圖表示)________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于酸堿中和滴定實驗的說法正確的是

A. 用圖B的滴定管可準確量取25.00 mL的酸性KMnO4溶液
B. 滴定過程中,眼睛要時刻注視滴定管中液面的變化
C. 滴定管裝入液體前不需用待裝液潤洗
D. 滴定前平視,滴定結束后仰視讀數,會使測定結果偏大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com