
【題目】已知下列熱化學方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ·mol-1
Fe2O3(s)+![]() CO(g)===
CO(g)===![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g) ΔH=-15.73 kJ·mol-1
CO2(g) ΔH=-15.73 kJ·mol-1
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=640.4 kJ·mol-1
則14gCO氣體還原足量FeO固體得到Fe固體和CO2氣體時對應的ΔH約為( )
A. -218 kJ·mol-1B. -109 kJ·mol-1
C. 218 kJ·mol-1D. 109 kJ·mol-1
 教材全解字詞句篇系列答案
教材全解字詞句篇系列答案科目:高中化學 來源: 題型:
【題目】對可逆反應4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列敘述中正確的是( )
4NO(g)+6H2O(g),下列敘述中正確的是( )
A.達到化學平衡時4υ正(O2)=5υ逆(NO)
B.若單位時間內生成xmolNO的同時,消耗xmolNH3,則反應達平衡狀態
C.達到化學平衡時,若升高溫度,則正反應速率減小,逆反應速率增大
D.平衡時混合物中可能各物質的濃度相等,且保持不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物P是合成抗腫瘤藥物的中間體,其合成路線如下:
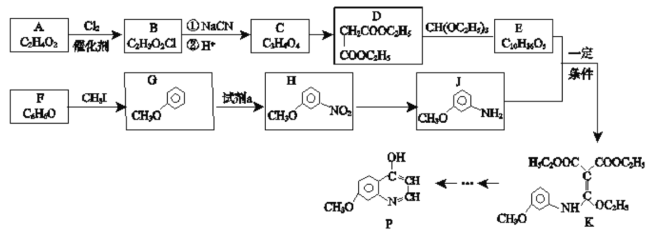
已知:RCl![]() RCOOH
RCOOH
(1)H的官能團名稱___________。寫出E的結構簡式___________。
(2)B→C中①的化學方程式___________。
(3)檢驗F中官能團的試劑及現象_________。
(4)D的同分異構體有多種,其中滿足以下條件的有________種。
①1mol D能與足量 NaHCO3反應放出2mol CO2
②核磁共振氫譜顯示有四組峰
(5)H→J的反應類型___________。
(6)已知: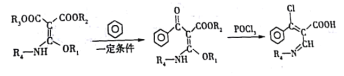
K經過多步反應最終得到產物P:
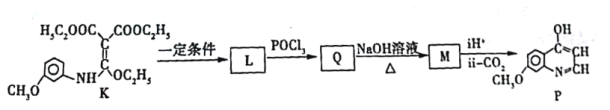
①K→L的化學方程式___________。
②寫出M的結構簡式___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉀和碘的相關化合物在化工、醫藥、材料等領域有著廣泛的應用。回答下列問題:
(1)元素K的焰色反應呈紫紅色,其中紫色對應的輻射波長為_______nm(填標號)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基態K原子中,核外電子占據的最高能層的符號是_________,占據該能層電子的電子云輪廓圖形狀為___________。K和Cr屬于同一周期,且核外最外層電子構型相同,但金屬K的熔點、沸點等都比金屬Cr低,原因是___________________________。
(3)X射線衍射測定等發現,I3AsF6中存在I3+離子。I3+離子的幾何構型為_____________,中心原子的雜化形式為________________。
(4)KIO3晶體是一種性能良好的非線性光學材料,具有鈣鈦礦型的立體結構,邊長為a=0.446nm,晶胞中K、I、O分別處于頂角、體心、面心位置,如圖所示。K與O間的最短距離為______nm,與K緊鄰的O個數為__________。
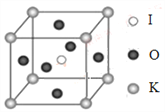
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】早期發現的一種天然二十面體準晶顆粒由Al、Cu、Fe 三種金屬元素組成,回答下列問題:
(1)準晶是一種無平移周期序,但有嚴格準周期位置序的獨特晶體,可通過_______方法區分晶體、準晶體和非晶體。
(2)基態 Fe原子有_______個未成對電子,Fe3+的電子排布式為 _____,可用硫氰化鉀檢驗Fe3+,形成的配合物的顏色為________ 。
(3)新制備的Cu(OH)2可將乙醛〔CH3CHO)氧化成乙酸,而自身還原成Cu2O。乙醛中碳原子的雜化軌道類型為____________,乙酸的沸點明顯高于乙醛,其主要原因是________。Cu2O為半導體材料,在其立方晶胞內部有4個氧原子,其余氧原子位于面心和頂點,則該晶胞中有_______個銅原子。
(4)Al單質為面心立方晶體,其晶胞參數a=0.405nm,晶胞中鋁原子的配位數為_____ 。列式表示Al單質的密度___________g·cm-3(不必計算出結果)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是()
A.Ca(HCO3)2溶液與少量NaOH溶液反應:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
B.用銅作電極電解食鹽水:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.向氧化鐵中加入氫碘酸:Fe2O3+6H+=2Fe3++3H2O
D.向一定量明礬溶液中滴加Ba(OH)2溶液至生成沉淀的物質的量最多:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學工作者研發了一種 SUNCAT的系統,借助鋰循環可持續,合成其原理如圖所示。下列說法不正確的是
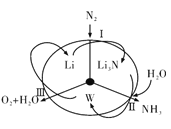
A. 過程I得到的Li3N的電子式為![]()
B. 過程Ⅱ生成W的反應為Li3N+3H2O=3LiOH+NH3↑
C. 過程Ⅲ涉及的陽極反應為4OH--4e-=O2↑+2H2O
D. 過程I、Ⅱ、Ⅲ均為氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A,B,C,D,E,F均為周期表中前36號元素,且原子序數依次增大.A,B,C為同一周期的主族元素,B原子p能級電子總數與s能級電子總數相等.A,F原子未成對電子是同周期中最多的,且F基態原子中電子占據三種不同形狀的原子軌道.D和E原子的第一至第四電離能如下表所示:
電離能/kJ·mol-1 | I1 | I2 | I3 | I4 |
D | 738 | 1451 | 7733 | 10540 |
E | 578 | 1817 | 2745 | 11578 |
(1)A,B,C三種元素的電負性最大的是__(填寫元素符號),D,E兩元素中D的第一電離能較大的原因是__.
(2)F基態原子的核外電子排布式是__;在一定條件下,F原子的核外電子從基態躍遷到激發態產生的光譜屬于__光譜(填“吸收”或“發射”).
(3)根據等電子原理,寫出AB+的電子式:__.
(4)已知:F3+可形成配位數為6的配合物.組成為FCl36H2O的配合物有3種,分別呈紫色、藍綠色、綠色,為確定這3種配合物的成鍵情況,分別取等質量的紫色、藍綠色、綠色3種物質的樣品配成溶液,分別向其中滴入過量的AgNO3溶液,均產生白色沉淀且質量比為3:2:1.則綠色配合物的化學式為__.
A [CrCl(H2O)5]Cl2H2O B [CrCl2(H2O)4]Cl2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]3H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com