
| A. | 標準狀況下,11.2L的O2和NO的混合物含有的分子數約為0.5×6.02×1023 | |
| B. | 1mol的羥基與1 mol的氫氧根離子所含電子數均為9 NA | |
| C. | 常溫常壓下42g 乙烯和丁烯混合氣體中,碳氫鍵的數目為6NA | |
| D. | 6.4g SO2與3.2g氧氣反應生成SO3,轉移電子數為0.2NA |
分析 A.一氧化氮與氧氣反應生成二氧化氮,導致混合氣體的分子數減少;
B.羥基中含有9個電子,氫氧根離子含有10個電子;
C.烯烴中極性鍵為碳氫鍵,乙烯和丁烯的最簡式為CH2,根據最簡式計算出混合物中含有碳氫鍵數目;
D.二氧化硫與氧氣生成三氧化硫的反應為可逆反應,反應物不可能完全轉化成生成物.
解答 解:A.標準狀況下,11.2L混合氣體的物質的量為0.5mol,由于O2和NO反應生成二氧化氮,導致氣體分子數減少,混合物含有的分子數小于0.5×6.02×1023,故A錯誤;
B.1mol的羥基中含有9mol電子,1 mol的氫氧根離子含有10mol電子,所含電子數不同,故B錯誤;
C.42g乙烯和丁烯的混合物中含有3mol最簡式CH2,含有6mol氫原子,烯烴中極性鍵為碳氫鍵,6mol氫原子形成了6mol碳氫極性鍵,所以混合氣體中含有極性鍵數為6NA,故C正確;
D.6.4g二氧化硫的物質的量為0.1mol,0.1mol二氧化硫與氧氣反應,由于該反應為可逆反應,則反應生成的三氧化硫小于0.1mol,轉移的電子小于0.2mol,轉移電子數小于0.2NA,故D錯誤;
故選C.
點評 本題考查阿伏加德羅常數的有關計算和判斷,題目難度中等,注意掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系,明確可逆反應特點,選項B為易錯點,注意羥基與氫氧根離子的區別.


科目:高中化學 來源: 題型:多選題
| A. | 取a克混合物充分加熱至質量不變,減重b克 | |
| B. | 取a克混合物與足量稀硝酸充分反應,加熱、蒸干、灼燒至熔化,冷卻得b克固體 | |
| C. | 取a克混合物與足量稀硫酸充分反應,逸出氣體用堿石灰完全吸收,增重b克 | |
| D. | 取a克混合物與足量Ba(OH)2溶液充分反應,過濾、洗滌、烘干,得b克固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
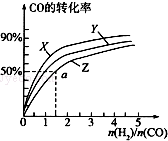 甲醇是重要的燃料,有廣闊的應用前景:工業上一般以CO和為原料合成甲醇,該反應的熱化學方程式為:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1
甲醇是重要的燃料,有廣闊的應用前景:工業上一般以CO和為原料合成甲醇,該反應的熱化學方程式為:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 加入適量銅粉除去Cu(NO3)2溶液中的AgNO3雜質 | |
| B. | 用NaOH溶液除去CO2中混有的HCl氣體 | |
| C. | 稀釋濃硫酸時,應將濃硫酸沿器壁慢慢倒入量筒中的水中 | |
| D. | 用乙醇從碘水中萃取碘 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 分子組成相差1個或若干個CH2原子團的物質互稱為同系物 | |
| B. | 相對分子質量相同的有機物是同分異構體 | |
| C. | 分子式相同、結構相同的有機物物理性質和化學性質一定相同 | |
| D. | 碳原子之間只以單鍵相結合的鏈烴為烷烴 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com