
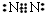 ;
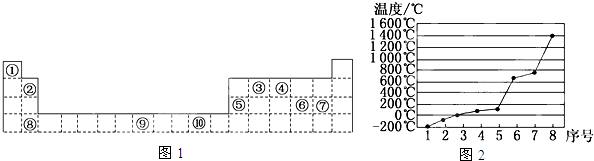
;分析 由元素在周期表中位置,可知①為H、②為Be、③為C、④為N、⑤為Al、⑥為S、⑦為Cl、⑧為Ca、⑨為Fe、⑩為Cu.
(1)d區元素包括ⅢB-ⅦB元素,Ⅷ族元素,為第3列到10列元素(鑭系元素、錒系元素除外);
(2)⑨為Fe元素,屬于26號元素,根據核外電子排布規律書寫基態原子的電子排布式;
(3)s能級最多容納2個電子,同一能層中s能級填滿后再填充p能級,故n=2,該元素的特征電子排布式為2s2np3,為N元素;
(4)元素④的氫化物為NH3,分子中N一直在形成3個N-H鍵,還含有1對孤對電子;
(5)第3周期8種元素中Si是原子晶體,單質的熔點最高;第三周期中氯元素電負性最大,常溫下氯氣、氬氣為氣體,氯氣比氬氣的相對分子質量大,熔點僅高于氬氣.
解答 解:由元素在周期表中位置,可知①為H、②為Be、③為C、④為N、⑤為Al、⑥為S、⑦為Cl、⑧為Ca、⑨為Fe、⑩為Cu.
(1)d區元素包括ⅢB-ⅦB元素,Ⅷ族元素,為第3列到10列元素(鑭系元素、錒系元素除外),由元素在周期表中位置可知,⑨處于第8列,為第Ⅷ族元素,屬于d區的元素,
故答案為:⑨;
(2)由元素在周期表中的位置可知,⑨為Fe元素,屬于26號元素,基態原子的電子排布式為1S22S22P63S23P63d64S2,
故答案為:1S22S22P63S23P63d64S2;
(3)s能級最多容納2個電子,同一能層中s能級填滿后再填充p能級,故n=2,該元素的特征電子排布式為2s2np3,s能級為成對電子,p能級3個電子個占據1個軌道,故該元素原子的核外最外層電子的成對電子為1對,為N元素,單質電子式為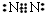 ,
,
故答案為:1;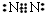 ;
;
(4)元素④的氫化物為NH3,分子中N一直在形成3個N-H鍵,還含有1對孤對電子,空間構型為三角錐形,N原子采取,sp3雜化,
故答案為:三角錐形;sp3;
(5)第3周期8種元素中Si是原子晶體,單質的熔點最高;同周期自左而右電負性增強,第三周期中Cl元素的電負性最大,氯氣常溫下為氣體,比氬氣的相對分子質量大,熔點僅高于氬氣,故2代表氯元素,
故答案為:Si;2.
點評 本題考查元素周期表的結構、核外電子排布規律、晶體結構與性質、電負性等,難度不大,整體把握元素周期表的結構,注意晶體類型與物質熔沸點高低比較.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
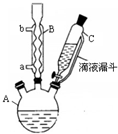 對氯苯甲酸是合成非甾族消炎鎮痛藥的中間體,還能用于燃料和濃藥的合成,實驗室中制備對氯苯甲酸的反應、裝置圖如圖:
對氯苯甲酸是合成非甾族消炎鎮痛藥的中間體,還能用于燃料和濃藥的合成,實驗室中制備對氯苯甲酸的反應、裝置圖如圖: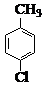 $→_{催化劑}^{KMnO_{4}}$
$→_{催化劑}^{KMnO_{4}}$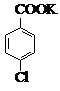 +MnO2
+MnO2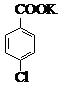
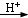
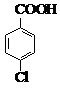
| 熔點/℃ | 沸點/℃ | 密度/g•cm-3 | 顏色 | 水溶性 | |
| 對氯甲苯 | 7.5 | 162 | 1.07 | 無色 | 難溶 |
| 對氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 對氯苯甲酸鉀 | 具有鹽的通性,屬于可溶性鹽 | ||||
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
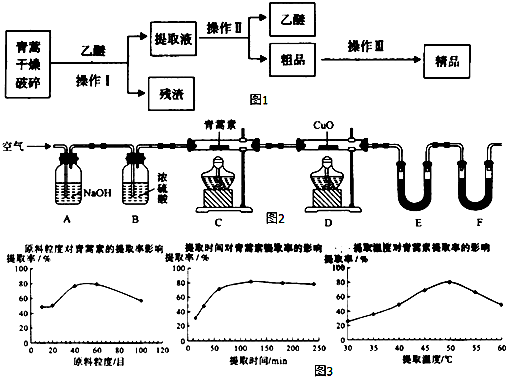
| 裝置 | 實驗前/g | 實驗后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 物質 | 雜質 | 除雜試劑或操作方法 |
| ① | NaCl溶液 | Na2CO3 | 加入鹽酸,蒸發 |
| ② | FeSO4溶液 | CuSO4 | 加入過量鐵粉并過濾 |
| ③ | H2 | CO2 | 依次通過盛有NaOH溶液和濃硫酸的洗氣瓶 |
| ④ | NaNO3 | CaCO3 | 加稀鹽酸溶解、過濾、蒸發、結晶 |
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
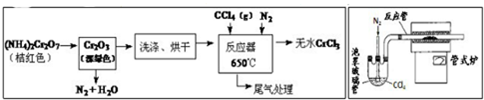
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 全球氣候變暖可能是由于二氧化碳含量的急劇增加 | |
| B. | 酸雨可以分為硫酸型酸雨和硝酸型酸雨 | |
| C. | 居室中的裝潢材料緩慢釋放出來的污染物中最常見的是甲醛、苯等有機物蒸氣 | |
| D. | 檢驗居室中甲醛氣體是否存在,可以抽取并通過品紅溶液來檢驗 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

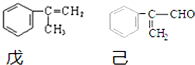
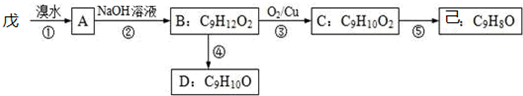
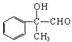
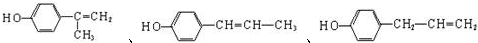 .
.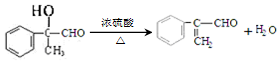 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com