
| A. | 某澄清透明溶液中:K+、Cu2+、NO3-、Cl- | |
| B. | 含0.1mol•L-1 Fe3+的溶液中:Na+、Mg2+、SO42-、Cl-、SCN- | |
| C. | 含0.1mol•L-1 CO32-的溶液中:OH-、Cl-、NH4+、Na+、H+ | |
| D. | 加入鋁粉產生H2的溶液中:Al3+、Na+、SO42-、NO3- |
分析 A.四種離子之間不反應,能夠共存;
B.鐵離子與硫氰根離子反應;
C.碳酸根離子、氫氧根離子、銨根離子都與氫離子反應;
D.該溶液中存在大量氫離子或氫氧根離子,鋁離子與氫氧根離子反應,硝酸根離子在酸性條件下與鋁反應不會生成氫氣.
解答 解:A.K+、Cu2+、NO3-、Cl-之間不反應,為澄清透明溶液,故A正確;
B.Fe3+、SCN-之間反應生成硫氰化鐵,在溶液中不能大量共存,故B錯誤;
C.CO32、OH-、NH4+都與H+發生反應,在溶液中不能大量共存,故C錯誤;
D.加入鋁粉產生H2的溶液呈酸性或堿性,溶液中存在大量氫離子或氫氧根離子:Al3+與氫氧根離子反應,NO3-在酸性條件下與鋁反應不會生成氫氣,在溶液中一定不能大量共存,故D錯誤;
故選A.
點評 本題考查離子共存的正誤判斷,為高考的高頻題,屬于中等難度的試題,注意明確離子不能大量共存的一般情況:能發生復分解反應的離子之間;能發生氧化還原反應的離子之間;能發生絡合反應的離子之間(如 Fe3+和 SCN-)等;還應該注意題目所隱含的條件,如:溶液的酸堿性,據此來判斷溶液中是否有大量的 H+或OH-;溶液的具體反應條件,如“氧化還原反應”、“加入鋁粉產生氫氣”;是“可能”共存,還是“一定”共存等;試題側重對學生基礎知識的訓練和檢驗,有利于提高學生靈活運用基礎知識解決實際問題的能力.


 全優考典單元檢測卷及歸類總復習系列答案
全優考典單元檢測卷及歸類總復習系列答案科目:高中化學 來源: 題型:選擇題
| A. | 中子數為34,質子數為29的銅原子:${\;}_{34}^{63}$Cu | |
| B. | 碳原子的結構示意圖: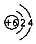 | |
| C. | 二氧化碳的電子式: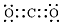 | |
| D. | 乙醇的結構簡式:CH3CH2OH |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol C3H8氣體中含有共價鍵數目為11NA | |
| B. | 1mol Na2O和Na2O2混合物中含有的陰陽離子總數是3NA | |
| C. | 將0.1mol氯化鐵溶于1L水中,所得溶液含有0.1NA個Fe3+ | |
| D. | 標準狀況下,22.4L氯氣與足量氫氧化鈉溶液反應轉移的電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
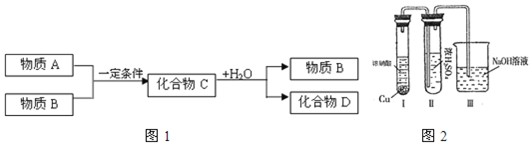
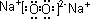 ;化合物D中所含化學鍵的類型是共價鍵、離子鍵.
;化合物D中所含化學鍵的類型是共價鍵、離子鍵.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(H+)=0.1mol/L的溶液:Na+、NH4+、SO42-、CO32- | |
| B. | 堿性溶液:Cu2+、NO3-、Fe3+、SO42- | |
| C. | 與鋁粉反應放出H2的無色溶液:NO3-、Al3+、Na+、SO42- | |
| D. | 使紅色石蕊試紙變藍的溶液:SO42-、CO32-、Na+、K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com