
分析 (1)根據電子轉移守恒計算金屬化合價最簡單整數比;
(2)A、B兩種金屬元素的相對原子質量之比是8:9,設金屬的相對原子質量分別為8x、9x,B的物質的量為3y,2y,A、B金屬的化合價分別為m、n,結合化合價關系、電子轉移守恒、混合物總質量列方程討論計算.
解答 解:(1)A、B金屬的化合價分別為m、n,二者反應生成氫氣體積相等,根據電子轉移守恒則3m=2n,故m:n=2:3,
故答案為:2:3;
(2)設A、B金屬的相對原子質量分別為8x、9x,A、B的物質的量為3y,2y,
A、B金屬的化合價分別為m、n,二者反應生成氫氣體積相等,根據電子轉移守恒則3m=2n,
反應共生成0.06mol 氫氣,根據電子轉移守恒則:3y×m+2y×n=0.06×2
由混合物總質量,可得:8x×3y+9x×2y=1.26,
聯立三個式子,可得x=n,
則當n=1時,金屬A的相對原子質量為8,不符合;
當n=2時,金屬A的相對原子質量為16,不符合;
當n=3時,金屬A的相對原子質量為24,金屬B的相對原子質量為27,符合;
即A的摩爾質量為24g/mol,B的摩爾質量為27g/mol,
答:A的摩爾質量為24g/mol,B的摩爾質量為27g/mol.
點評 本題考查金屬與酸的反應、化學方程式有關計算,注意電子守恒與討論法的運用,在討論時應注意常見金屬的化合價為+1、+2、+3.


科目:高中化學 來源: 題型:選擇題
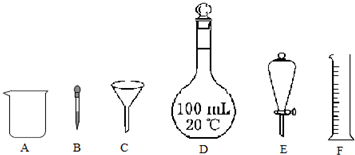
| A. | 將金屬鈉在研體中研成粉末,使鈉與水反應的實驗更安全 | |
| B. | 用pH試紙測定溶液的pH時,需先用蒸餾水潤濕試紙 | |
| C. | 分液時,分液漏斗內的上層液體應由上口倒出 | |
| D. | 用滴定管取液時,開始和最后讀數時均俯視,則量取的體積準確 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ①③④ | C. | ①③⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 液面在“0”刻度時,25mL堿式滴定管和50mL堿式滴定管所盛溶液的體積 | |
| B. | 在過氧化鈉固體中,陰離子與陽離子的個數 | |
| C. | 將質量分數為a%的H2SO4溶液蒸發水后變為2a%,蒸發前后H2SO4溶液的物質的量濃度 | |
| D. | 在碳與濃硫酸(加熱)的反應中,被還原的H2SO4與參加反應的H2SO4的物質的量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,1L液態水中含有的H+數目為10-7 NA | |
| B. | 標準狀況下,2.24 L D2O中含有的電子數為NA | |
| C. | 3.4g H2O2中含有的共用電子對數為0.1 NA | |
| D. | 1mol碳烯(:CH2)中含有的電子數為8NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向溴化亞鐵溶液中通入過量氯氣:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- | |
| B. | 碳酸氫鎂中加過量氫氧化鈉:Mg2++2HCO3-+2OH-=MgCO3↓+CO32-+2H2O | |
| C. | 向過氧化氫酸性溶液中加入氯化亞鐵:2Fe2++2H++H2O2=2Fe3++2H2O | |
| D. | 明礬溶液中加入過量的氨水A13++3NH3•H20=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
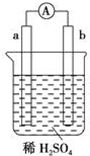
| A. | 碳棒上有氣體放出,溶液pH變大 | |
| B. | a是正極,b是負極 | |
| C. | 稀硫酸中有電子流動,方向是從b極到a極 | |
| D. | a極上發生了氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2、8、18、32、72、98 | B. | 2、8、8、18、18、32 | C. | 2、8、8、18、32、32 | D. | 2、8、18、32、32、72 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com