
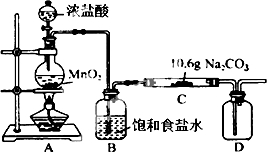
 某化學活動小組設計如圖所示(部分夾持裝置已略去)實驗裝置,以探究潮濕的Cl2與Na2CO3反應得到的固體物質.
某化學活動小組設計如圖所示(部分夾持裝置已略去)實驗裝置,以探究潮濕的Cl2與Na2CO3反應得到的固體物質.| 步驟 | 預期現(xiàn)象和結論 |
| 步驟1:取C中少量樣品于試管中,滴加足量蒸餾水 至溶解,然后將所得溶液分別置于A、B試管中 | 固體物質全部完全溶解 |
| 步驟:向A試管中滴加適量BaCl溶液 | a. 如果 b. 如果 |
| 步驟: | 有白色沉淀生成,C的部分有NaCl |
分析 (1)二氧化錳與濃鹽酸在加熱條件下反應生成氯氣、氯化錳和水;
(2)氯氣有毒,直接排放能夠引起空氣污染,圖中實驗裝置缺少尾氣處理裝置;
(3)步驟2中向A試管中滴加適量BaCl2溶液,是檢驗產(chǎn)物中是否有Na2CO3,回答該小題時要結合最后的結論,a應為證明固體中不含Na2CO3,b應為證明固體中含Na2CO3,不能顛倒,步驟3應是檢驗氯離子,應向B試管中滴加過量的稀硝酸,再滴加AgNO3溶液,若溶液變渾濁,證明固體中含有NaCl;
分別假設分析計算,依據(jù)氧化還原反應電子守恒計算判斷氯元素化合價寫出化合物化學式.
解答 解:(1)二氧化錳與濃鹽酸在加熱條件下反應生成氯氣、氯化錳和水,化學方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)氯氣有毒,直接排放能夠引起空氣污染,應進行尾氣處理,所以應在裝置D后連接以尾氣處理裝置;
故答案為:在裝置D后連接以尾氣處理裝置;
(3)步驟2中向A試管中滴加適量BaCl2溶液,是檢驗產(chǎn)物中是否有Na2CO3,最后的結論:a.若無明顯現(xiàn)象,證明固體中不含Na2CO3;
b.若溶液變渾濁,證明固體中含Na2CO3;
步驟3應是檢驗氯離子,應向B試管中滴加過量的稀硝酸,再滴加AgNO3溶液,若溶液變渾濁,證明固體中含有NaCl;
C中有0.1mol Cl2參加反應.裝置C中通入一定量的氯氣后,測得D中只有一種常溫下為黃紅色的氣體,若假設一成立,反應為Cl2+Na2CO3→NaHCO3+NaCl+X,依據(jù)氧化還原反應電子守恒計算判斷氯元素化合價為+1價:可推知C中反應生成的含氯氧化物為Cl2O;反應的化學方程式為:2Cl2+H2O+2Na2CO3=2NaHCO3+2NaCl+Cl2O;
故答案為:a.若無明顯現(xiàn)象,證明固體中不含Na2CO3;
B.若溶液變渾濁,證明固體中含Na2CO3;
步驟3:向B試管中滴加過量的稀硝酸,再滴加AgNO3溶液;
Cl2O; 2Cl2+2Na2CO3+H2O═2NaCl+2NaHCO3+Cl2O.
點評 本題考查了物質性質驗證的實驗設計,步驟分析判斷,掌握物質性質和實驗設計方法是解題關鍵,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 除去SO2中的少量HCl:通入飽和NaHSO3溶液的洗氣瓶,干燥后收集氣體 | |
| B. | FeCl2溶液中混有FeCl3:加入過量鐵粉充分反應后過濾 | |
| C. | Na2CO3固體中混有少量NaHCO3:加入適量NaOH溶液 | |
| D. | 除去SiO2中的少量Al2O3:加入適量稀硫酸充分反應后過濾 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某溶液中滴加AgNO3溶液有白色沉淀,說明原溶液中有Cl- | |
| B. | 某溶液中先滴加足量鹽酸無規(guī)象,再滴加BaCl2溶液有白色沉淀.則原溶液中有SO42- | |
| C. | 某無色溶液滴入酚酞試液顯紅色,該溶液一定是含有大量的H+ | |
| D. | 某溶液中滴加鹽酸生成能使澄清石灰水變渾濁的無色氣體,說明原溶液中有CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Cu2+、Cl-、NO3- | B. | Na+、K+、SO32-、CO32- | ||
| C. | K+、HCO3-、NO3-、Cl- | D. | Ca2+、Mg2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com