
| A. | 25℃時,CH3COOH與CH3COONa的混合溶液,若測得混合液pH=6,則溶液中:c(CH3COO-)<c(Na+) | |
| B. | 為確定某酸H2A是強酸還是弱酸,可測NaHA溶液的pH.若pH>7,則H2A是弱酸;若pH<7,則H2A是強酸 | |
| C. | 足量鋅分別和等體積、等物質的量濃度的鹽酸和醋酸反應時產生H2的量相等,放出H2的速率不等 | |
| D. | 相同溫度下,將足量氯化銀固體分別放入相同體積的①蒸餾水、②0.1mol/L鹽酸、③0.1mol/L氯化鎂溶液、④0.1 mol/L硝酸銀溶液中,Ag+濃度:①>④=②>③ |
分析 A.混合溶液顯酸性,則c(H+)>c(OH-),結合電荷守恒分析;
B.NaHA溶液的pH<7,可能是HA-的電離程度大于水解程度;
C.醋酸為弱酸,不能完全電離;
D.氯化銀難溶于水,在水中的溶解度很小,一定溫度下,溶液中Ksp(AgCl)=c(Ag+)•c(Cl-)為定值,溶液中c(Cl-)越大,c(Ag+)越小.
解答 解:A.混合溶液顯酸性,則c(H+)>c(OH-),溶液中電荷守恒為c(H+)+c(Na+)=c(OH-)+c(CH3COO-),則c(CH3COO-)>c(Na+),故A錯誤;
B.NaHA溶液的pH<7,可能是HA-的電離程度大于水解程度,所以H2A可能是弱酸,故B錯誤;
C.醋酸為弱酸,不能完全電離,等體積、等物質的量濃度的鹽酸和醋酸反應時產生H2的量相等,但反應的速率不等,故C正確;
D.氯化銀難溶于水,在水中的溶解度很小,一定溫度下,溶液中Ksp(AgCl)=c(Ag+)•c(Cl-)為定值,①蒸餾水中沒有氯離子、②0.1mol/L鹽酸中c(Cl-)=0.1mol/L,③0.1 mol/L氯化鎂溶液c(Cl-)=0.2mol/L、④0.1mol/L硝酸銀溶液中c(Ag+)=0.1mol/L,溶液中c(Ag+)為④>①>②>③,故D錯誤.
故選:C.
點評 本題考查強弱電解質、弱電解質的電離、鹽類水解、溶度積及相關計算等,難度中等,注意把握強弱電解質關鍵是電解質是否完全電離以及溶度積常數的應用,側重于考查學生的分析能力和應用能力.


科目:高中化學 來源: 題型:實驗題
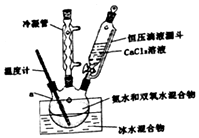 過氧化鈣(CaO2)是一種白色結晶體粉末,極微溶于水,不溶于醇類、乙醚等,加熱至150℃左右開始分解放出氧氣,與水緩慢反應生成H2O2.易于酸反應生成H2O2
過氧化鈣(CaO2)是一種白色結晶體粉末,極微溶于水,不溶于醇類、乙醚等,加熱至150℃左右開始分解放出氧氣,與水緩慢反應生成H2O2.易于酸反應生成H2O2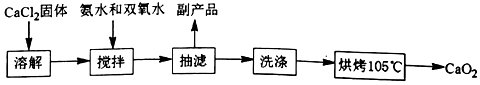
| 數據 時間 | 樣品取用質量/(g) | 平均消耗體積(KMnO4)/mL |
| 放置前測定 | a | 25.00 |
| 放置一個月后測定 | a | 24.00 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某溶液中加入硝酸銀溶液時,生成白色沉淀,說明溶液中有Cl- | |
| B. | 某溶液中加入稀硫酸溶液時,生成無色氣體,說明溶液中有CO32- | |
| C. | 某溶液中加入氯化鋇溶液時,生成白色沉淀,說明溶液中有SO42- | |
| D. | 某溶液中加入鹽酸溶液,無明顯現象,再加入氯化鋇溶液時,生成白色沉淀,說明溶液中有SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩種溶液中的c(Na+)相等 | |
| B. | 分別加熱到相同溫度時,CH3COONa溶液的pH大 | |
| C. | 分別加水稀釋到100 mL時,兩種溶液的pH依然相等 | |
| D. | 兩溶液中由水電離出的c(OH-)之比為$\frac{1{0}^{-5}}{1{0}^{-9}}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
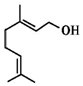
| A. | 不能使溴的四氯化碳溶液褪色 | B. | 香葉醇的分子式為C10H20O | ||
| C. | 不能使酸性高錳酸鉀溶液褪色 | D. | 能發生取代反應和加成反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol NaHCO3晶體中含有NA個CO32- | |
| B. | 標準狀況下,11.2L的18O2中所含的中子數為8NA | |
| C. | 1mol Fe與足量的稀HNO3反應,轉移電子數目為3NA | |
| D. | 標準狀況下,22.4L苯中含有碳氫鍵數目為6NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
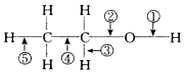
| A. | 與濃硫酸混合加熱至170℃,斷②⑤ | B. | 與氫鹵酸反應斷② | ||
| C. | 分子間脫水斷①或② | D. | 與醋酸反應斷② |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com