

分析 金屬A焰色反應為黃色,故A為Na,由反應Na+水→氣體甲+D,故甲為H2,D為NaOH,由NaOH+金屬B→H2可知,B為Al,乙是黃綠色氣體,則乙為Cl2,由甲+乙→丙,故丙為HCl,HCl溶于水的物質E,故E為鹽酸;H為紅褐色沉淀,由G+NaOH→H,則H為Fe(OH)3,G含有Fe3+,由E(鹽酸)$\stackrel{金屬(C)}{→}$F$\stackrel{Cl_{2}}{→}$G可知,C為Fe,F為FeCl2,G為FeCl3.
解答 解:金屬A焰色反應為黃色,故A為Na,由反應Na+水→氣體甲+D,故甲為H2,D為NaOH,由NaOH+金屬B→H2可知,B為Al,乙是黃綠色氣體,則乙為Cl2,由甲+乙→丙,故丙為HCl,HCl溶于水的物質E,故E為鹽酸;H為紅褐色沉淀,由G+NaOH→H,則H為Fe(OH)3,G含有Fe3+,由E(鹽酸)$\stackrel{金屬(C)}{→}$F$\stackrel{Cl_{2}}{→}$G可知,C為Fe,F為FeCl2,G為FeCl3.
(1)由上述分析可知,A為Na,H為Fe(OH)3,G為FeCl3,乙為Cl2,
故答案為:Na;Fe(OH)3;FeCl3;Cl2;
(2)反應①的離子方程式為:Fe+2H+═Fe2++H2↑,
反應②的離子方程式為:2OH-+2Al+2H2O═2AlO2-+3H2↑,
反應③的離子方程式為:2 Fe2++Cl2═2Fe3++2 Cl-,
故答案為:Fe+2H+═Fe2++H2↑;2OH-+2Al+2H2O═2AlO2-+3H2↑;2 Fe2++Cl2═2Fe3++2 Cl-.
點評 本題考查無機物的推斷,注意特殊的顏色與特殊反應是推斷的突破口,需要學生熟練掌握元素化合物知識,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | CH4+2O2 $\stackrel{點燃}{→}$CO2+2H2O | B. | CH2=CH2+Br2→CH2BrCH2Br | ||
| C. | 2C2H5OH+2Na→2C2H5ONa+H2↑ | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 如圖A 直流電源,B為浸透飽和氯化鈉溶液和酚酞試液的濾紙,C為電鍍槽,接通電路后,發現B上的c點顯紅色,請填空
如圖A 直流電源,B為浸透飽和氯化鈉溶液和酚酞試液的濾紙,C為電鍍槽,接通電路后,發現B上的c點顯紅色,請填空查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | BaO2、NaCl、LiH 三種物質陽離子與陰離子個數比均為:1:1 | |
| B. | CCl4、NH3、PCl3中所有原子都滿足最外層為8電子結構 | |
| C. | 甲烷可與溴水發生取代反應,乙烯可與溴水發生加成反應 | |
| D. | 燃料電池是通過燃燒所釋放的熱能再轉化為電能的裝置 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素代號 | X | Y | Z | W |
| 原子半徑/nm | 0.186 | 0.160 | 0.102 | 0.074 |
| 主要化合價 | +1 | +2 | -2、+4、+6 | -2 |
| A. | X、Y元素的金屬性X<Y | |
| B. | X和W能組成兩種化合物 | |
| C. | Y和W屬于同周期的元素 | |
| D. | Z和W屬于同主族元素,其單質能直接化合生成ZW3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 棉花、蠶絲和錦綸的主要成分是纖維素 | |
| B. | 油脂在空氣中完全燃燒生成二氧化碳和水 | |
| C. | 苯、乙醇和乙酸都能發生取代反應 | |
| D. | 淀粉和纖維素的組成通式為(C6H10O5)n,二者互為同分異構體 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
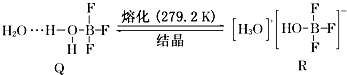
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化銨和過氧化氫的分解 | B. | 二氧化硅與二氧化碳的熔化 | ||
| C. | 蔗糖和干冰的熔化 | D. | 氯化鎂和氯化鋁的熔化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com