
 (1)某氣態有機物X含C、H、O三種元素,已知下列條件,現欲確定X的分子式,所需的最少條件組合是①②④.(填相應的數字序號)
(1)某氣態有機物X含C、H、O三種元素,已知下列條件,現欲確定X的分子式,所需的最少條件組合是①②④.(填相應的數字序號)分析 (1)根據各元素質量分數與相對分子質量可以確定有機物分子式;
(2)濃H2SO4增重14.4g為水的質量,堿石灰增重26.4g為二氧化碳質量,計算各自物質的量,結合有機物總質量判斷是否含有元素,再計算各原子數目之比,進而確定實驗式;
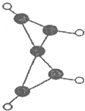
(3)①由結構模型可知,分子中含有5個C原子、4個H原子;
②連接H原子的4個碳原子化學環境相同,與環交點碳原子環境不同;
③由碳的四價結構可知,三元環中連接H原子的碳原子之間含有碳碳雙鍵,而環交點碳原子連接的4個碳原子形成四面體結構;
④三元環中連接H原子的碳原子之間含有碳碳雙鍵.
解答 解:(1)根據各元素質量分數與相對分子質量可以計算分子式中各原子數目,可以確定有機物分子式,
故答案為:①②④;
(2)濃H2SO4增重14.4g為水的質量,水的物質的量為$\frac{14.4g}{18g/mol}$=0.8mol,n(H)=1.6mol,堿石灰增重26.4g為二氧化碳質量,其物質的量為$\frac{26.4g}{44g/mol}$=0.6mol,n(C)=0.6mol,有機物中n(O)=$\frac{12g-0.6mol×12g/mol-1.6mol×1g/mol}{16g/mol}$=0.2mol,故有機物中C、H、O原子數目之比為0.6:1.6:0.2=3:8:1,則有機物實驗式為C3H8O,
故答案為:C3H8O;
(3)①由結構模型可知,分子中含有5個C原子、4個H原子,該物質分子式為:C5H4,故答案為:C5H4;
②連接H原子的4個碳原子化學環境相同,與環交點碳原子環境不同,有2種化學環境不同的碳原子,故答案為:2;
③由碳的四價結構可知,三元環中連接H原子的碳原子之間含有碳碳雙鍵,而環交點碳原子連接的4個碳原子形成四面體結構,三元環中3個碳原子共面,故答案為:3;
④三元環中連接H原子的碳原子之間含有碳碳雙鍵,故答案為:碳碳雙鍵.
點評 本題考查有機物分子式確定、有機物結構等,理解掌握有機物分子式確定方法,注意實驗式與分子式的不同,烴及烴的含氧衍生物中H原子飽和碳的四價結構時,實驗式即為分子式.


科目:高中化學 來源: 題型:選擇題
| A. | 用電解法精煉粗銅時,粗銅作陽極 | |
| B. | 在原電池中,銅電極只能作正極 | |
| C. | 在鍍件上鍍銅時,金屬銅作陽極 | |
| D. | 鋅銅原電池(稀硫酸為電解質溶液),銅極上發生還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、K+、SO42-、Cl- | B. | Na+、ClO-、SO42-、Fe2+ | ||
| C. | Ba2+、K+、HCO3-、NO3- | D. | Ba2+、Na+、SO42-、SO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液中.Na+一定存在,且濃度為0.1mol/L | |
| B. | 該溶液中CO32-和SO42-一定存在,且物質的量濃度均為0.1mol/L | |
| C. | Ba2+一定不存在 | |
| D. | NH4+ 一定存在,且100mL溶液中物質的量為0.02mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
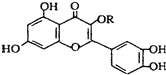
| A. | 可與溴水反應,且1 mol該物質與足量溴水反應耗6 mol Br2 | |
| B. | 可與NaOH溶液反應,1 mol該物質可與5 mol NaOH反應 | |
| C. | 一定條件下1 mol該物質與H2加成耗H2最大量為8 mol | |
| D. | 維生素P遇FeCl3溶液發生顯色反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
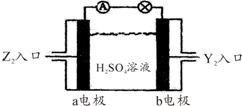 已知X、Y和Z三種元素的原子序數之和等于42.X元素原子的4p軌道上有3個未成對電子,Y元素原子的最外層2p軌道上有2個未成對電子.X跟Y可形成化合物X2Y3,Z元素可以形成負一價離子.請回答下列問題:
已知X、Y和Z三種元素的原子序數之和等于42.X元素原子的4p軌道上有3個未成對電子,Y元素原子的最外層2p軌道上有2個未成對電子.X跟Y可形成化合物X2Y3,Z元素可以形成負一價離子.請回答下列問題: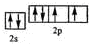 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高溫度,可以使純水中的c(H+)>c(OH-) | |
| B. | 在NaOH溶液中沒有H+,在HCl溶液中沒有OH- | |
| C. | 水的電離過程是一個吸熱過程 | |
| D. | 將水加熱,KW增大,pH不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
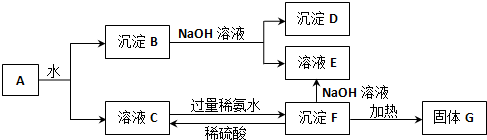
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

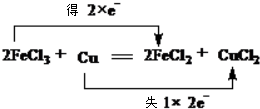 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com