
| A. | 加少量燒堿固體 | B. | 升高溫度 | ||
| C. | 加少量冰醋酸 | D. | 加少量醋酸鈉固體 |
分析 要使溶液中中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大,應是平衡向電離的方向移動,結合影響平衡移動的因素解答該題.
解答 解:A.加入燒堿溶液,反應生成CH3COO-,c(H+)減小,c(OH-)增大,Ka=$\frac{c(C{H}_{3}CO{O}^{-})×c({H}^{+})}{c(C{H}_{3}COOH)}$不變,c(CH3COO-)增大,則$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$減小,故A錯誤;
B.弱電解質的電離為吸熱過程,加熱促進電離,c(H+)增大,c(CH3COOH)減小,則$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大,故B正確;
C.加少量冰醋酸,醋酸濃度增大,弱電解質的濃度越大,電離程度越小,則$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$減小,故C錯誤;
D.加少量醋酸鈉固體,電離平衡逆向移動,則氫離子濃度減小,醋酸濃度增大,則$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$減小,故D錯誤.
故選B.
點評 本題考查弱電解質的電離,側重于考查學生的分析能力和化學基本概念的理解和應用能力,難度不大,注意把握影響弱電解質的電離的影響因素.


科目:高中化學 來源: 題型:解答題
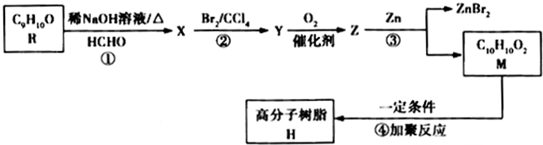
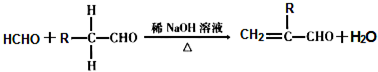
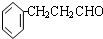 .
.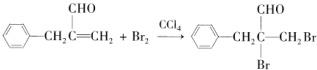 .
.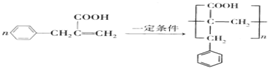 .
.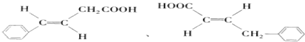 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
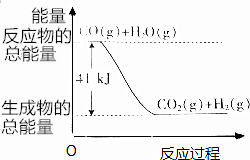 CO(g)+H2O(g)?CO2(g)+H2(g)反應的能量變化如圖所示.下列反應既是氧化還原反應,又是放熱反應的是( )
CO(g)+H2O(g)?CO2(g)+H2(g)反應的能量變化如圖所示.下列反應既是氧化還原反應,又是放熱反應的是( )| A. | 鎂條在氧氣中燃燒 | B. | 木炭與CO2反應 | ||
| C. | 硝酸和氫氧化鋇溶液反應 | D. | CO2(g)+H2(g)=CO(g)+H20(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在Na2A、NaHA兩溶液中,離子種類不相同 | |
| B. | 在溶質的物質的量相等的Na2A,NaHA兩溶液中,陰離子總數相等 | |
| C. | 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-) | |
| D. | 在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向血紅色的Fe(SCN)3溶液中加入少量KI 固體,溶液顏色變淺 | |
| B. | 氨水溶液加水稀釋,c(OH-)增大,平衡常數增大 | |
| C. | pH=12的Na0H和Na2S溶液中水的電離程度前者大于后者 | |
| D. | 25℃,Cu(OH)2在水中的溶度積和溶解度比其在Cu(NO3)2溶液中的大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電離程度 | B. | 醋酸的電離常數 | ||
| C. | 中和時所需NaOH的物質的量 | D. | CH3COOH的物質的量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入少量Ca(OH)2固體 | B. | 加水稀釋 | ||
| C. | 加入少量NaOH固體 | D. | 加少量的Na2CO3固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
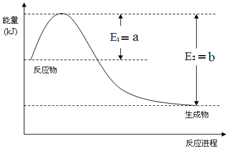 運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義
運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com