
| A. | 純堿溶液顯堿性,可用熱的純堿溶液除去金屬表面的油污 | |
| B. | 明礬溶于水可形成氫氧化鋁膠體,可用于自來水的殺菌消毒 | |
| C. | NH3溶于水后顯堿性,在FeCl3飽和溶液中通入足量NH3可制取Fe(OH)3膠體 | |
| D. | 氫氧化鐵的溶解度比氫氧化銅的小得多,可向硫酸銅溶液中加入氫氧化鐵除去混有的Cu2+ |
分析 A、碳酸鈉水解顯堿性,水解是吸熱反應,利用此點性質可以除去油污;
B、明礬只能凈水不能消毒;
C、在FeCl3飽和溶液中通入足量NH3得到Fe(OH)3沉淀;
D、沉淀容易由溶解度大的向溶解度小的轉化.
解答 解:A、碳酸鈉水解顯堿性,而水解是吸熱反應,故熱的純堿溶液的水解程度更大,堿性更強,由于油脂能在堿性條件下水解,故可以用熱的純堿溶液去油污,故A正確;
B、明礬不具有強氧化性,可水解生成膠體凈化水,但不能消毒殺菌,故B錯誤;
C、在FeCl3飽和溶液中通入足量NH3得到Fe(OH)3沉淀,應在沸水中滴加FeCl3飽和溶液制備Fe(OH)3膠體,故C錯誤;
D、氫氧化鐵的溶解度比氫氧化銅的小得多,而沉淀容易由溶解度大的向溶解度小的轉化,故沉淀容易由氫氧化銅轉化為氫氧化鐵,即可向硫酸鐵溶液中加入氫氧化銅除去混有的Fe3+,故D錯誤.
故選A.
點評 本題考查了物質的用途,性質決定用途,熟悉碳酸鈉、明礬的性質是解題關鍵,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 其他步驟正確,滴定達到終點時,俯視讀數,測得c(H+)偏大 | |
| B. | 實驗測得25℃時,HgI2的Ksp=4×10-9 | |
| C. | 一定溫度下,向HgI2飽和溶液中加入少量Hg(NO3)2溶液,HgI2的Ksp減小 | |
| D. | 溫度不變,在t時,向HgI2飽和溶液中加入少量濃KI溶液,離子濃度變化如圖所示 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
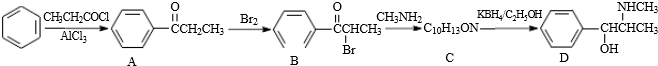
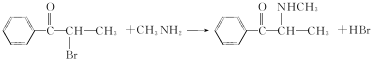 .C-D的反應類型為還原反應.
.C-D的反應類型為還原反應.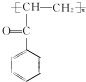
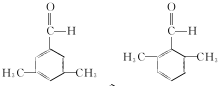 (寫結構簡式).
(寫結構簡式). 參照上述合成路線,設計一條由苯和乙酸為起始原料制備
參照上述合成路線,設計一條由苯和乙酸為起始原料制備 的合成路線:
的合成路線: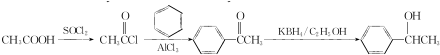 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| CH4 (g) | H2O (g) | CO (g) | H2 (g) |
| 3.0mol•L-1 | 8.5mol•L-1 | 2.0mol•L-1 | 2.0mol•L-1 |
| 實驗序號 | 溫度/℃ | 壓強/kPa | v(CH4)/mol•L-1•s-1 | v(H2O)/mol•L-1•s-1 |
| 1 | 360 | P1 | 0.100 | 0.100 |
| 2 | 480 | 101 | 0.120 | 0.120 |
| 3 | 360 | P2 | 0.080 | 0.080 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1NH4HS溶液中有:c(NH4+)=c(HS-)+c(S2-)+c(H2S) | |
| B. | 25℃時,將a mol•L-1的氨水與0.01mol•L-1的鹽酸等體積混合后,c(NH4+)=c(Cl-),則NH3•H2O的電離常數為$\frac{1{0}^{-9}}{a-0.01}$ | |
| C. | 等濃度的HCN和NaCN混合溶液中有:2c(Na+)=c(CN-)+c(HCN) | |
| D. | 等pH的①(NH4)2SO4溶液 ②NH4HSO4溶液 ③NH4Cl溶液中,c(NH4+)的大小關系:①=③>② |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵與鹽酸反應,鐵合金不與鹽酸反應 | |
| B. | 一定條件下,鐵粉可與水蒸氣反應 | |
| C. | 不銹鋼是鐵合金,只含金屬元素 | |
| D. | 純鐵的硬度和強度均高于鐵合金 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2的水溶液能導電,所以SO2是電解質 | |
| B. | 酸式鹽的水溶液呈酸性 | |
| C. | 鹽類水解是中和反應的逆反應 | |
| D. | 凡是強酸生成的鹽,其水溶液呈中性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com