
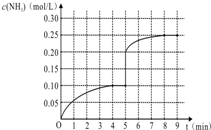
 在一容積為1L的密閉容器內加入0.1mol的N2和0.3mol的H2,在一定條件下發生如下反應:N2(g)+3H2(g)?2NH3(g)△H<0,反應中NH3的物質的量濃度的變化情況如圖:
在一容積為1L的密閉容器內加入0.1mol的N2和0.3mol的H2,在一定條件下發生如下反應:N2(g)+3H2(g)?2NH3(g)△H<0,反應中NH3的物質的量濃度的變化情況如圖:分析 (1)化學平衡常數K等于生成物濃度冪之積與反應物濃度冪之積的比;
(2)先計算氨氣反應速率,再根據同一可逆反應中同一段時間內各物質的反應速率之比等于其計量數之比計算氮氣反應速率;
(3)可逆反應達到平衡狀態時,正逆反應速率相等,反應體系中各物質的物質的量、物質的量濃度、百分含量以及由此引起的一系列物理量不變;
(4)改變條件的一瞬間,氨氣濃度增大,隨著反應的進行,氨氣濃度增大平衡正向移動.
解答 解:(1)該反應化學平衡常數K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$,
故答案為:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$;
(2)v(NH3)=$\frac{0.10-0}{4}$mol/(L.min)=0.025 mol/(L•min),同一可逆反應中同一段時間內各物質的反應速率之比等于其計量數之比,所以v(N2)=$\frac{1}{2}$ v(NH3)=$\frac{1}{2}$×0.025 mol/(L•min)=0.0125 mol/(L•min),
故答案為:0.0125 mol/(L•min);
(3)a.N2和NH3濃度相等時,該反應不一定達到平衡狀態,與反應初始濃度及轉化率有關,所以不能據此判斷平衡狀態,故錯誤;
b.NH3百分含量保持不變時,正逆反應速率相等,反應達到平衡狀態,故正確;
c.容器中氣體的壓強不變時,正逆反應速率相等,反應體系中各物質的物質的量不變,反應達到平衡狀態,故正確;
d.當2v正(H2)=32v逆(NH3) 時反應達到平衡狀態,所以當 3v正(H2)=2v逆(NH3)時反應沒有達到平衡狀態,故錯誤;
故選:b、c;
(4)改變條件的一瞬間,氨氣濃度增大,隨著反應的進行,氨氣濃度增大平衡正向移動,只能是增大壓強平衡正向移動,故答案為:增大壓強.
點評 本題考查化學平衡計算、化學平衡狀態判斷、化學平衡影響因素等知識點,側重考查學生分析判斷及計算能力,“反應前后改變的物理量不變時”可逆反應達到平衡狀態,注意分析圖象中曲線變化趨勢與外界影響因素的關系,題目難度不大.


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:選擇題
| A. | 向澄清石灰水中通入足量二氧化碳:2OH?+CO2═CO32?+H2O | |
| B. | 氧化鈉投入水中發生反應:O2?+H2O═2OH? | |
| C. | 醋酸溶液滴入到NaOH溶液中:CH3COOH+OH?═CH3COO?+H2O | |
| D. | 鐵和稀鹽酸反應制氫氣:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
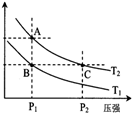 甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上一般可采用如下反應來合成甲醇(于固定容器中進行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上一般可采用如下反應來合成甲醇(于固定容器中進行):2H2(g)+CO(g)?CH3OH(g)| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AgCl不能轉化為AgI | |
| B. | 25℃時,0.1mol/L HF溶液pH=l | |
| C. | 25℃時,使AgCl轉化為AgI,則加入KI溶液的濃度不低于5×10-12mol/L | |
| D. | 向1L0.1mol/LHF溶液中加入1L 0.1mol/LCaCl2溶液,沒有沉淀產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電池放電時,電池負極周圍溶液的pH 不斷增大 | |
| B. | 電池充電時,陽極反應為:Ni(OH)2+OH--e-═NiO(OH)+H2O | |
| C. | 電池充電時,氫元素被氧化 | |
| D. | 電池放電時,負極反應為:H2-2e-═2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵與硫酸銅溶液反應:Fe+Cu2+═Fe2++Cu | |
| B. | 氧化鎂與稀鹽酸混合:MgO+H+═Mg2++H2O | |
| C. | 碳酸鈣與鹽酸反應:CO32-+2H+═CO2↑+H2O | |
| D. | 氫氧化鋇溶液與稀硫酸反應:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C(Na+)=2C(S2-)+2C(HS-)+2C(H2S) | B. | C(Na+)+C(H+)=C(OH-)+C(HS-)+C(S2-) | ||
| C. | C(OH-)=C(H+)+C(HS-)+2(H2S) | D. | C(Na+)>C(S2-)>C(OH-)>C(HS-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com