
| A. | ②⑤ | B. | ③④⑤ | C. | ①②⑤ | D. | ④⑥ |
分析 ①生成物質量增大小于混合物總質量增大,生成物的質量分數可能降低;
②平衡向正反應移動,生成物的物質的量一定增加;
③增大某一反應的濃度,平衡向正反應移動,其它反應物的轉化率增大,自身轉化率降低;
④如增大反應物的濃度,平衡向正方向移動,達到平衡時,反應物的濃度比改變條件前大;
⑤平衡向正反應移動,正反應速率一定大于逆反應速率;
⑥加入催化劑不影響化學平衡.
解答 解:①總質量不變,向正反應移動,生成物的質量分數一定增大,但是若加入反應物,導致生成物質量增大小于混合物總質量增大,生成物的質量分數可能降低,故①錯誤;
②平衡向正反應移動,生成物的物質的量一定增加,則生成物的產量一定增加,故②正確;
③若增大某一反應的濃度,平衡向正反應移動,其它反應物的轉化率增大,加入的反應物的轉化率降低,故③錯誤;
④如增大反應物的濃度,平衡向正方向移動,達到平衡時,反應物的濃度會增大,故④錯誤;
⑤平衡向正反應移動,正反應速率一定大于逆反應速率,故⑤正確;
⑥加入催化劑,正、逆反應速率同等程度增大,化學平衡不移動,故⑥錯誤;
綜上所述正確為:②⑤,
故選A.
點評 本題考查化學平衡的影響因素,題目難度中等,注意掌握影響化學平衡移動的因素,解答時注意從勒沙特列原理的角度分析.


科目:高中化學 來源: 題型:選擇題
| A. | 具有吸附性 | |
| B. | 溶解度大于CuS、PbS、CdS | |
| C. | 溶解度小于CuS、PbS、CdS | |
| D. | MnO2的氧化性強于Cu2+、Pb2+、Cd2+等金屬離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將氯氣與通入冷的消石灰中反應制漂白粉:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | |
| B. | 向較濃的Na2SiO3溶液中滴加適量鹽酸制得硅酸膠體:Na2SiO3+2HCl═2NaCl+H2SiO3(膠體) | |
| C. | 鐵在潮濕的環境中生銹:3Fe+4H2O═Fe3O4+4H2↑ | |
| D. | 用氫氟酸刻蝕玻璃:SiO2+4HF═SiF4+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
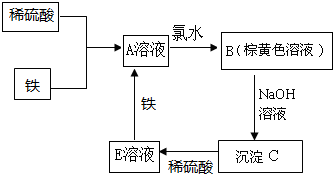 下列物質轉化關系如圖所示,反應過程中部分產物可能已略去請回答以下問題:
下列物質轉化關系如圖所示,反應過程中部分產物可能已略去請回答以下問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單位時間內消耗amol(A),同時消耗3amolC時,反應處于平衡狀態 | |
| B. | 增大容器的體積,化學平衡不移動,反應速率也不變 | |
| C. | 升高溫度使c(B)增大,可知正反應為放熱反應 | |
| D. | 加入催化劑,改變了反應歷程,但反應的△H不會變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子最外層電子數:X>Y>Z | B. | 離子半徑:W3+>Y2- | ||
| C. | 原子序數:X+M>Y+W | D. | 單質沸點:M>Z>Y |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 甲醇-空氣燃料電池(DMFC)是一種高效能、輕污染的車載電池,其工作原理如圖.下列有關敘述不正確的是( )
甲醇-空氣燃料電池(DMFC)是一種高效能、輕污染的車載電池,其工作原理如圖.下列有關敘述不正確的是( )| A. | H+從負極區通過交換膜移向正極區 | |
| B. | 正極的電極反應式為:O2+H2O+4e-═4OH- | |
| C. | 圖中a、b、c、d物質分別是CO2、CH2OH、H2O | |
| D. | 用該燃料電池電解飽和食鹽水,產生1.5mol氯氣,需要消耗甲醇16克 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com