
分析 ①1 mol五種烴分別完全燃燒,都生成CO2為$\frac{134.4L}{22.4L/mol}$=6mol,則分子中均含有6個C原子,且烴C完全燃燒時,生成的水的物質的量比CO2多,則生成的水應大于6mol,故分子中H原子數目大于12,由于為烷烴時H原子數目最大為14,故烴C的分子式為C6H14,符合③中C不與溴水或酸性KMnO4溶液反應;
②A和D都能使溴水褪色,含有碳碳不飽和鍵,其中1 mol D可以和1 mol H2反應生成1 mol A;1 mol A又可繼續和1 mol H2反應生成1 mol C,則D中含有2個碳碳雙鍵或者1個碳碳三鍵,A中含有1個碳碳雙鍵,故D的分子式為C6H10,A的分子式為:C6H12,
④A存在多種同分異構體,其中C只能由一種A與氫氣反應而得,則C為CH3CH2C(CH3)3,則A為CH2=CHC(CH3)3,則D為CH≡CC(CH3)3;
⑤B在鐵屑存在下可以與液溴反應,但不與溴水或酸性高錳酸鉀溶液反應,則B為苯( );
);
⑥B能與氫氣充分反應生成E為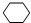 .
.
解答 解:①1 mol五種烴分別完全燃燒,都生成CO2為$\frac{134.4L}{22.4L/mol}$=6mol,則分子中均含有6個C原子,且烴C完全燃燒時,生成的水的物質的量比CO2多,則生成的水應大于6mol,故分子中H原子數目大于12,由于為烷烴時H原子數目最大為14,故烴C的分子式為C6H14,符合③中C不與溴水或酸性KMnO4溶液反應;
②A和D都能使溴水褪色,含有碳碳不飽和鍵,其中1 mol D可以和1 mol H2反應生成1 mol A;1 mol A又可繼續和1 mol H2反應生成1 mol C,則D中含有2個碳碳雙鍵或者1個碳碳三鍵,A中含有1個碳碳雙鍵,故D的分子式為C6H10,A的分子式為:C6H12,
④A存在多種同分異構體,其中C只能由一種A與氫氣反應而得,則C為CH3CH2C(CH3)3,則A為CH2=CHC(CH3)3,則D為CH≡CC(CH3)3;
⑤B在鐵屑存在下可以與液溴反應,但不與溴水或酸性高錳酸鉀溶液反應,則B為苯( );
);
⑥B能與氫氣充分反應生成E為 .
.
(1)由上述分析可知,A屬于烯烴,B屬于芳香烴,C屬于烷烴,
故答案為:烯烴;芳香烴;烷烴;
(2)C為CH3CH2C(CH3)3,分子中含有3種H原子,則烴C的一鹵代產物有3種同分異構體,
故答案為:3;
(3)D為CH≡CC(CH3)3,名稱為:3,3-二甲基-1-丁炔,
故答案為:3,3-二甲基-1-丁炔;
(4)烯烴、炔烴能與溴發生加成反應,以上物質能作為溴水中溴的萃取劑的有:苯、烷烴、環烷烴,
故答案為:BCE;
(5)符合題設條件的A與HCl在催化劑作用下的加成反應方程式:CH2=CHC(CH3)3+HCl$\stackrel{催化劑}{→}$ClCH2CH2C(CH3)3,
故答案為:CH2=CHC(CH3)3+HCl$\stackrel{催化劑}{→}$ClCH2CH2C(CH3)3.
點評 本題考查有機物的推斷,屬于描述型題目,關鍵是根據燃燒生成二氧化碳與水的量確定C的分子式,再結合發生的反應推斷,側重考查學生的分析推理能力.


 習題精選系列答案
習題精選系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
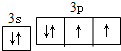 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用鋼瓶儲存液氯或濃硫酸 | |
| B. | 通過灼熱的銅網以除去H2中混有的O2 | |
| C. | Cu與濃硫酸反應終止后,冷卻,向試管中加適量蒸餾水以觀察水合銅離子的顏色 | |
| D. | 用廣泛pH試紙測得某溶液的pH為3.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 陰極:2H++2e-=H2↑ 陽極:4OH--4e-=2H2O+O2↑ | |
| B. | 陰極:Cu2++2e-=Cu 陽極:4OH--4e-=2H2O+O2↑ | |
| C. | 陰極:2H++2e-=H2↑ 陽極:2Cl--2e-=Cl2↑ | |
| D. | 陰極:Cu2++2e-=Cu 陽極:2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 14組 | B. | 20組 | C. | 26組 | D. | 32組 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
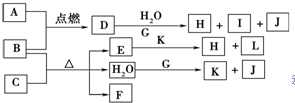 如圖中,A到L為常見物質或該物質的水溶液,B在A氣體中燃燒產生棕色煙,B、G為中學化學中常見金屬單質,H為紅褐色沉淀,I的焰色反應為黃色,組成J的元素原子核內只有一個質子,F為無色、有刺激性氣味氣體,且能使品紅溶液褪色.
如圖中,A到L為常見物質或該物質的水溶液,B在A氣體中燃燒產生棕色煙,B、G為中學化學中常見金屬單質,H為紅褐色沉淀,I的焰色反應為黃色,組成J的元素原子核內只有一個質子,F為無色、有刺激性氣味氣體,且能使品紅溶液褪色.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時電解質溶液的密度減小 | B. | 放電時K+向Cd極區移動 | ||
| C. | 充電時陽極Cd元素被氧化 | D. | 充電時陰極附近的pH增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com