
| A. | 根據同周期元素的第一電離能變化趨勢,推出Al的第一電離能比Mg大 | |
| B. | 根據主族元素最高正化合價與族序數的關系,推出鹵族元素最高正價都是+7 | |
| C. | 根據同周期元素的電負性變化趨勢,推出Ar的電負性比Cl大 | |
| D. | 根據較強酸可以制取較弱酸的規律,推出CO2通入NaClO溶液中能生成HClO |
分析 A.Mg的3s全滿,為穩定結構;
B.F沒有正價;
C.Ar為稀有氣體,性質穩定;
D.CO2通入NaClO溶液中,發生強酸制取弱酸的反應.
解答 解:A.同周期元素的第一電離能從左向右增大,而Mg的3s全滿,為穩定結構,則Al的第一電離能比Mg小,故A錯誤;
B.主族元素最高正化合價與族序數的關系,而鹵族元素中除F外最高正價都是+7,故B錯誤;
C.同周期元素的電負性從左向右增大,而Ar的電負性比Cl小,Cl易得到電子,可知同周期中鹵素原子的電負性最大,故C錯誤;
D.CO2通入NaClO溶液中,發生強酸制取弱酸的反應,規律合理,故D正確;
故選D.
點評 本題考查較綜合,涉及元素周期律、物質結構與性質,為高頻考點,把握電負性、電離能的比較方法及元素的性質、酸性比較為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 乙烯酮在一定條件下能與含活潑氫的化合物發生加成:它與下列試劑發生加成反應時所生成的產物不正確的是( )
乙烯酮在一定條件下能與含活潑氫的化合物發生加成:它與下列試劑發生加成反應時所生成的產物不正確的是( )| A. | 與HCl加成生成CH3COCl | B. | 與H2O加成生成CH3COOH | ||
| C. | 與CH3OH加成生成CH3COCH2OH | D. | 與CH3COOH加成生成(CH3CO)2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 萃取時,要求萃取劑的密度比水的密度大 | |
| B. | 蒸餾時,溫度計水銀球與蒸餾燒瓶支管口相平 | |
| C. | 過濾時,要將待過濾混合物轉移到漏斗中 | |
| D. | 分液時,分液漏斗的下口必須緊貼在燒杯壁上 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 周期表是按各元素的相對原子質量遞增的順序從左到右排列的 | |
| B. | 元素周期表共有16個族,也就是16個縱行 | |
| C. | 同周期元素的電子層數相同 | |
| D. | 每一周期的元素都是從堿金屬開始,以稀有氣體結束 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Sr能與水反應,生成氫氣 | |
| B. | Sr(OH)2具有兩性 | |
| C. | SrSO4在水中溶解度很小 | |
| D. | SrCl2溶液和Na2CO3溶液能發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定是金屬元素 | |
| B. | 一定是ⅡA族元素 | |
| C. | 一定是非金屬元素 | |
| D. | 可能是金屬元素也可能是非金屬元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
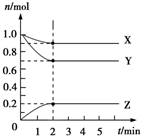 Ⅰ.控制變量法是化學實驗的一種常用方法.下表是某學習小組研究等物質的量濃度的稀硫酸和鋅反應的實驗數據,分析以下數據,回答下列問題:
Ⅰ.控制變量法是化學實驗的一種常用方法.下表是某學習小組研究等物質的量濃度的稀硫酸和鋅反應的實驗數據,分析以下數據,回答下列問題:| 序號 | 硫酸的體積/mL | 鋅的質量/g | 鋅的形狀 | 溫度/℃ | 完全溶于酸的時間/s | 生成硫酸鋅的質量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 顆粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 顆粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 燃料電池工作時O2在正極上發生氧化反應 | |
| B. | 燃料電池在工作時需要點燃甲烷 | |
| C. | 燃料電池工作時燃料在負極上發生氧化反應 | |
| D. | 燃料電池工作時負極的電極反應式為:2H2O+O2+4e-=4OH- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com