
| A. | NaCl、NaOH、NH4NO3、CaCO3 | B. | FeCl3、CuSO4、Mg(OH)2、NaCl | ||
| C. | BaSO4、AgCl、KOH、NH4Cl | D. | NH4HCO3、MgCl2、BaCl2、Ba(NO3)2 |
分析 A.只有碳酸鈣不溶于水,NaCl溶于水熱效應不明顯,NaOH溶于水放熱、NH4NO3溶于水吸熱;
B.FeCl3溶于水為黃色,CuSO4溶于水為藍色,Mg(OH)2不溶于水、NaCl溶于水;
C.BaSO4、AgCl均不溶于水;
D.均溶于水得到無色溶液,且熱效應不明顯.
解答 解:A.只有碳酸鈣不溶于水,NaCl溶于水熱效應不明顯,NaOH溶于水放熱、NH4NO3溶于水吸熱,利用水可鑒別,故A選;
B.FeCl3溶于水為黃色,CuSO4溶于水為藍色,Mg(OH)2不溶于水、NaCl溶于水,溶于水現象不同,可鑒別,故B選;
C.BaSO4、AgCl均不溶于水,現象相同,用水不能鑒別,故C不選;
D.均溶于水得到無色溶液,且熱效應不明顯,現象相同,用水不能鑒別,故D不選;
故選AB.
點評 本題考查物質的鑒別和檢驗,為高頻考點,把握物質的性質、溶于水的現象為解答的關鍵,側重分析與應用能力的考查,注意元素化合物知識的應用,題目難度不大.


 能考試期末沖刺卷系列答案
能考試期末沖刺卷系列答案科目:高中化學 來源: 題型:選擇題
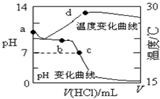 室溫下,將1.000mol/L鹽酸滴入20.00mL1.000mol/L氨水中,溶液pH和溫度隨加入鹽酸體積變化曲線如圖所示.下列有關說法正確的是( )
室溫下,將1.000mol/L鹽酸滴入20.00mL1.000mol/L氨水中,溶液pH和溫度隨加入鹽酸體積變化曲線如圖所示.下列有關說法正確的是( )| A. | a點由水電離出的c(H+)=1.0×10-14mol/L | |
| B. | b點時c(NH4+)+c(NH3•H2O)=c(Cl-) | |
| C. | c點時消耗的鹽酸體積:V(HCl)<20.00mL | |
| D. | d點后,溶液溫度略下降的主要原因是NH3•H2O電離吸熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
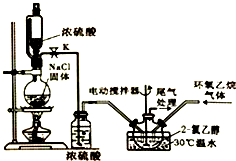 2-氯乙醇是一種重要的有機化工原料,受熱時易分解.通常是以適量的2-氯乙醇為溶劑,用氯化氫與環氧乙烷反應制得新的2-氯乙醇.制取反應裝置如圖所示.
2-氯乙醇是一種重要的有機化工原料,受熱時易分解.通常是以適量的2-氯乙醇為溶劑,用氯化氫與環氧乙烷反應制得新的2-氯乙醇.制取反應裝置如圖所示.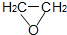 (g)+HCl(g)?ClCH2CH2OH(l)△H<0
(g)+HCl(g)?ClCH2CH2OH(l)△H<0| 化合物名稱 | 相對分子質量 | 熔點(℃) | 沸點(℃) |
| 環氧乙烷 | 44 | -112,2 | 10.8 |
| 2-氯乙醇 | 80.5 | -67.5 | 128.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 甲圖中的小黑點疏密表述電子在核外空間出現機會的大小 | |
| B. | 甲圖中的每個小黑點表示1個電子 | |
| C. | 乙圖表示1s電子只能在球體內出現 | |
| D. | 乙圖表明1s軌道呈圓形,有無數對稱軸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com