
| A、10 mL質量分數為98%的H2SO4,用水稀釋至100 mL,H2SO4的質量分數為9.8% |
| B、在H2O2+Cl2=2HCl+O2反應中,每生成32 g氧氣,則轉移2 NA個電子 |
| C、標準狀況下,分子數為NA的CO、C2H4混合氣體體積約為22.4 L,質量為28 g |
| D、一定溫度下,1 L 0.50 mol?L-1NH4Cl溶液與2 L 0.25mol?L-1NH4Cl溶液含NH4+物質的量不同 |
| m |
| M |
| 32g |
| 16g/mol |


 仁愛英語同步練習冊系列答案
仁愛英語同步練習冊系列答案 學習實踐園地系列答案
學習實踐園地系列答案科目:高中化學 來源: 題型:
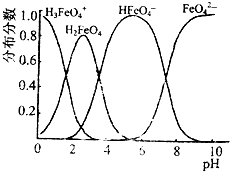 高鐵酸鈉的化學式為Na2FeO4,按要求回答下列問題:
高鐵酸鈉的化學式為Na2FeO4,按要求回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| A、甲醛(HCHO) |
| B、CO |
| C、氡(Rn) |
| D、NO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、v(A)=0.15 mol?L-1?min-1 |
| B、v(B)=0.015 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(D)=0.45 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、標準狀況下,2.24LCO和CO2混合氣體中含有的碳原子數目為0.1NA |
| B、常溫下,2.3g Na完全與O2反應失去的電子數為0.1NA |
| C、100mL 18.4mol?L-1的硫酸與足量銅反應,生成二氧化硫的分子數小于0.92 NA |
| D、在密閉容器中加入1.5mol H2和0.5molN2,充分反應后可得到NH3分子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、碳酸氫鈉溶液中加入醋酸:CO32-+2H+=H2O+CO2↑ |
| B、稀硫酸中加入鐵粉:2Fe+6H+=2Fe3++3H2↑ |
| C、碳酸鈣中加入鹽酸:CO32-+2H+=H2O+CO2↑ |
| D、氫氧化鈉溶液中加入硫酸:H++OH-=H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
 某興趣小組同學進行乙醛的銀鏡反應實驗的操作步驟如下:
某興趣小組同學進行乙醛的銀鏡反應實驗的操作步驟如下:| 實驗變量 實驗序號 | 銀氨溶液的量/mL | 乙醛的量/滴 | 溫度/℃ | 反應混合液的pH | 出現銀鏡的時間/min |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com