
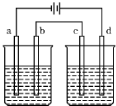
 按圖電解實驗裝置(都是惰性電極),若通直流電一段時間后,左池中溶液的pH上升,右池中溶液的pH下降,不僅a,b兩電極放電離子的物質的量相等,且b,c兩電極放電離子的物質的量也相等,則電解液應選用下表中的( )
按圖電解實驗裝置(都是惰性電極),若通直流電一段時間后,左池中溶液的pH上升,右池中溶液的pH下降,不僅a,b兩電極放電離子的物質的量相等,且b,c兩電極放電離子的物質的量也相等,則電解液應選用下表中的( )| 選項 | 左池 | 右池 |
| A | KCl | Cu(NO3)2 |
| B | AgNO3 | CuSO4 |
| C | NaCl | AgNO3 |
| D | KOH | CuSO4 |
| A、A | B、B | C、C | D、D |


科目:高中化學 來源: 題型:
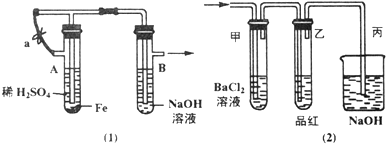
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
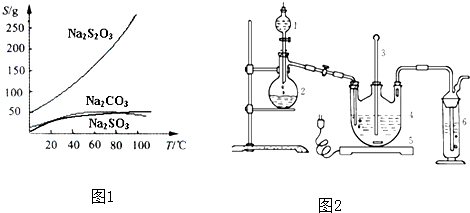
| ||
| 活性炭脫色 |
| 并保溫 |
| 操作① |
| 蒸發(fā)濃縮 |
| 冷卻晶體 |
| 操作② |
| 編號 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3標準溶液的體積/mL | 18.02 | 17.98 | 18.00 | 20.03 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 選項 | 理由 | 結論 |
| A | 與鹽酸反應時,相同物質的量的原子失去電子的數(shù)目:Al>Na | 還原性:Al>Na |
| B | 室溫時,相同物質的量濃度溶液的pH:AlCl3<MgCl2 | 堿性:Mg(OH)2>Al(OH)3 |
| C | 相同數(shù)目的分子可電離的H+數(shù):H2SO4>HClO4 | 酸性:H2SO4>HClO4 |
| D | 用飽和NaHCO3溶液可以除去CO2 中含有的少量SO2 | 非金屬性:S>C |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
 用如圖所示的收集裝置收集氨氣時,由于氣流略強使得在試管底部形成氣旋,導致氨氣與空氣混合而不能收集到純氨氣.現(xiàn)在有一小團棉花,請問將棉花放在試管那個位置可以阻止氣旋?請說明理由.
用如圖所示的收集裝置收集氨氣時,由于氣流略強使得在試管底部形成氣旋,導致氨氣與空氣混合而不能收集到純氨氣.現(xiàn)在有一小團棉花,請問將棉花放在試管那個位置可以阻止氣旋?請說明理由.查看答案和解析>>
科目:高中化學 來源: 題型:
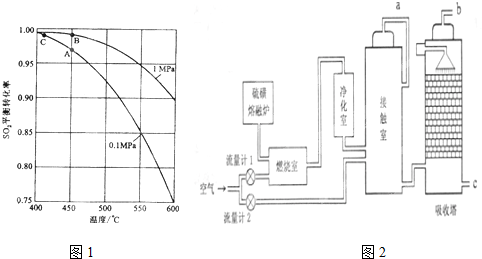
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、x值為2 |
| B、混合氣體的密度增大 |
| C、平衡時N的濃度為0.6 mol/L |
| D、N的轉化率為80% |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、氣體單質中一定含有共價鍵 |
| B、由非金屬元素組成的化合物一定是共價化合物 |
| C、含有離子鍵的晶體一定是離子晶體 |
| D、一定是在發(fā)生化學反應時,化學鍵才發(fā)生斷裂 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com