
| A. | 該反應的熱化學方程式為:2NH3?N2+3H2△H=-92kJ.mol-1 | |
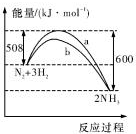
| B. | 生成物的能量之和比反應物的能量之和高 92 kJ | |
| C. | a曲線是未加入催化劑時的能量變化曲線 | |
| D. | 加入催化劑可增加正反應速率,減小逆反應速率 |
分析 A、熱化學方程式需要標注物質聚集狀態和對應焓變,選項中是反應的逆反應;
B、依據圖象分析,反應物能量高于生成物;
C、催化劑降低反應的活化能,改變反應速率不改變平衡;
D、催化劑同等程度改變反應正逆反應速率.
解答 解:A、該反應的熱化學方程式為:N2 (g)+3H2(g)?2NH3 (g)△H=-92KJ/mol,故A錯誤;
B、依據圖象可知,反應物能量之和比生成物的能量之和高92KJ,故B錯誤;
C、催化劑降低反應的活化能,改變反應速率不改變平衡,a曲線是未加入催化劑時的能量變化曲線,b曲線是加入催化劑時的能量變化曲線,故C正確;
D、加入催化劑可同等程度改變反應正逆反應速率,故D錯誤;
故選C.
點評 本題考查了阿伏伽德羅常數的應用,主要是熱化學方程式 書寫,圖象分析判斷,反應能量變化,催化劑作用分析,題目難度中等.


 全優考典單元檢測卷及歸類總復習系列答案
全優考典單元檢測卷及歸類總復習系列答案 品學雙優卷系列答案
品學雙優卷系列答案 小學期末沖刺100分系列答案
小學期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | 草酸稀溶液加水稀釋,溶液中所有離子濃度均減小 | |
| B. | NaHC2O4溶液中有:2c(Na+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-) | |
| C. | pH=3的草酸與pH=12的NaOH溶液混合至中性時,溶液中有:c(Na+)=c(HC2O4-)+2c(C2O42-) | |
| D. | 等濃度的草酸和碳酸相比,溶液中由水電離出來的c(H+)前者更多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在Na2S溶液中:c(Na+)=c(HS-)+c(S2-) | |
| B. | 乙烯的燃燒熱為akJ•mol-1(a>0),則乙烯燃燒的熱化學方程式可表示為C2H4(g)+3O2(g)=2CO2(g)+2H2O(g)△H=-akJ•mol-1 | |
| C. | 鋼鐵發生吸氧腐蝕的正極反應式為O2+4e-+2H2O=4OH- | |
| D. | 從酸化的海帶灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

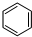 -CH3(g)+11H2△H=kJ•mol-1.
-CH3(g)+11H2△H=kJ•mol-1.查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3$→_{催化劑}^{O_{2}}$NO$\stackrel{O_{2}}{→}$ NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| B. | 濃縮海水$\stackrel{Cl_{2}}{→}$Br2$\stackrel{SO_{2}}{→}$ HBr$\stackrel{Cl_{2}}{→}$ Br2 | |
| C. | 飽和食鹽水$\stackrel{電解}{→}$Cl2$\stackrel{Ca(OH)_{2}}{→}$ 漂白粉 | |
| D. | H2和Cl2混合氣體$\stackrel{光照}{→}$HCl氣體$\stackrel{水}{→}$ 鹽酸 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com