
| A. | Na2SO4═Na++SO4-2 | B. | BaCl2═Ba2++Cl2- | ||
| C. | Al2(SO4)3═2Al3++3SO42- | D. | K2S═2K+S |
分析 A.硫酸根離子的表示方法不規范,且應該為2個鈉離子;
B.2g氯離子不能合并;
C.硫酸鋁在溶液中完全電離出鋁離子和硫酸根離子;
D.鉀離子和硫離子沒有標出所帶電荷.
解答 解:A.硫酸鈉為強電解質,完全電離,正確的電離方程式為:Na2SO4═2Na++SO42-,故A錯誤;
B.氯化鋇完全電離出鋇離子和氯離子,正確的電離方程式為:BaCl2═Ba2++2Cl-,故B錯誤;
C.硫酸鋁完全電離,其電離方程式為:Al2(SO4)3═2Al3++3SO42-,故C正確;
D.硫化鉀電離出鉀離子和硫離子,正確的電離方程式為:K2S═2K++S2-,故D錯誤;
故選C.
點評 本題考查了電離方程式的書寫方法,題目難度不大,明確電離方程式的書寫原則為解答關鍵,注意掌握強弱電解質的判斷方法,試題側重基礎知識的考查,培養了學生的規范答題能力.


科目:高中化學 來源: 題型:選擇題
| A. | 構成單質分子的粒子一定含共價鍵 | |
| B. | 非金屬元素組成的化合物一定不是離子化合物 | |
| C. | 第ⅠA族和第ⅦA族原子化合時一定形成離子鍵 | |
| D. | 共價化合物中一定不含離子鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol的羥基與1mol的氫氧根離子所含電子數均為9NA | |
| B. | 500mL0.1mol/L鹽酸中,含有HCl分子數目為0.05NA | |
| C. | 1molNa被氧化生成NaNO3水溶液或NaCl,都失去NA個電子 | |
| D. | 1.0L1.0mol•L-1的NaNO3水溶液中含有的氧原子數為3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 水起著溶解NH4NO3,發生吸熱現象以啟動反應的作用 | |
| B. | 每還原1molNO3需氧化1molZn和1molNH4+ | |
| C. | 成煙物質是兩性氧化物小顆粒 | |
| D. | 發煙物質是小鋅粒,它由NH4NO3反應放熱而蒸出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸和硫酸的濃度都增大 | B. | 鹽酸和硫酸的濃度都減大 | ||
| C. | 鹽酸的濃度減小,硫酸的濃度增大 | D. | 鹽酸的濃度增大,硫酸的濃度減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
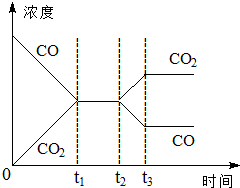 在一個恒容反應器中發生反應:CO(g)+H2O(g)?H2(g)+CO2(g),該反應的平衡常數隨溫度的變化如表:
在一個恒容反應器中發生反應:CO(g)+H2O(g)?H2(g)+CO2(g),該反應的平衡常數隨溫度的變化如表:| 溫度/℃ | 400 | 500 | 830 |
| 平衡常數K | 10 | 9 | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com