
 NaClO和KAl(SO4)2都是重要的化工產品,均可應用于造紙業.
NaClO和KAl(SO4)2都是重要的化工產品,均可應用于造紙業.分析 (1)NaClO為強堿弱酸鹽,水解呈堿性;
(2)NaClO溶液水解生成次氯酸具有強氧化性,可用于漂白;
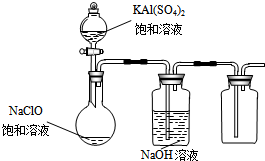
(3)①燒瓶中加入飽和KAl(SO4)2溶液,次氯酸根離子水解顯堿性,鋁離子水解顯酸性,混合后水解相互促進,產生大量的白色膠狀沉淀和次氯酸;
②將燒瓶中的混合液在陽光照射下,不久燒瓶中有黃綠色氣體產生.充分反應后集氣瓶中氣體能使帶余燼的木條復燃,依據現象分析是次氯酸分解生成氯氣、氧氣和水的反應;
(4)KAl(SO4)2溶液和Ba(OH)2溶液混合,當產生沉淀物質的量最多時,是鋁離子和鋇離子全部沉淀.
解答 解:(1)NaClO為強堿弱酸鹽,水解呈堿性,離子方程式為:ClO-+H2O?HClO+OH-,
故答案為:ClO-+H2O?HClO+OH-;
(2)NaClO溶液中次氯酸根離子水解生成次氯酸具有強氧化性,可用于漂白,故答案為:漂白紙漿;
(3)①向燒瓶中加入飽和KAl(SO4)2溶液,產生大量的白色膠狀沉淀,Al3+與ClO-發生互促水解反應,離子方程式為Al3++3ClO-+3H2O═3HClO+Al(OH)3↓,
故答案為:Al3++3ClO-+3H2O═3HClO+Al(OH)3↓;
②將燒瓶中的混合液在陽光照射下,不久燒瓶中有黃綠色氣體產生為氯氣,充分反應后集氣瓶中收集到一種無色無味的氣體為氧氣.依據氧化還原反應電子守恒寫出化學方程式配平得到:4HClO$\frac{\underline{\;光照\;}}{\;}$2H2O+2Cl2↑+O2↑;
故答案為:4HClO$\frac{\underline{\;光照\;}}{\;}$2H2O+2Cl2↑+O2↑;
(4)若將V1 mL 0.1mol/L KAl(SO4)2溶液和V2mL 0.1mol/LBa(OH)2溶液混合.當產生沉淀物質的量最多時,是鋁離子和鋇離子全部沉淀,反應的化學方程式為:2KAl(SO4)2+3Ba(OH)2=3BaSO4↓+2Al(OH)3↓+K2SO4,則0.1mol/L×V1:0.1mol/L×V2=2:3,V1:V2=2:3,
故答案為:2:3.
點評 本題考查鹽類水解知識,為高頻考點,側重于化學與生活、生產的考查,有利于培養學生良好的科學素養,提高學習的積極性,難度中等,注意相關基礎知識的積累.


科目:高中化學 來源: 題型:解答題
 噴泉是一種常見的自然現象,其產生的原因是存在壓強差.制取氨氣并完成噴泉實驗(圖中夾持裝置均已略去).
噴泉是一種常見的自然現象,其產生的原因是存在壓強差.制取氨氣并完成噴泉實驗(圖中夾持裝置均已略去).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,2NO(g)+O2(g)═2NO2(g)能夠自發進行,則該反應的△H<0 | |
| B. | 反應N2(g)+3H2(g)?2NH3(g),其他條件不變時充入N2,正反應速率增大,逆反應速率減小 | |
| C. | 同溫、同濃度的硫酸和氫氧化鈉稀溶液中,水的電離程度相同 | |
| D. | 硫酸工業中二氧化硫的催化氧化,不采用高壓是因為壓強對SO2轉化率無影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氯氣的實驗室制法是MnO2和濃鹽酸在加熱條件下反應,若將MnO2換成KMnO4、KClO3等氧化劑氧化濃鹽酸亦可快速制取氯氣.根據上述反應原理,有人提出猜想:能否利用Na2O2的強氧化性氧化濃鹽酸得到氯氣呢?某課外小組在實驗室進行了探索性實驗,設計了如圖所示裝置:
氯氣的實驗室制法是MnO2和濃鹽酸在加熱條件下反應,若將MnO2換成KMnO4、KClO3等氧化劑氧化濃鹽酸亦可快速制取氯氣.根據上述反應原理,有人提出猜想:能否利用Na2O2的強氧化性氧化濃鹽酸得到氯氣呢?某課外小組在實驗室進行了探索性實驗,設計了如圖所示裝置:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 工業上設計用CO2來生產燃料甲醇,既減少二氧化碳氣體,又得到寶貴的能源物質.為了探究反應原理,現進行如下實驗:在體積為1L的密閉容器中,充入1molCO2和3molH2,某溫度下發生反應:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-49.0KJ/mol.測得CO2和CH3OH(g)的濃度隨時間變化如圖所示
工業上設計用CO2來生產燃料甲醇,既減少二氧化碳氣體,又得到寶貴的能源物質.為了探究反應原理,現進行如下實驗:在體積為1L的密閉容器中,充入1molCO2和3molH2,某溫度下發生反應:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-49.0KJ/mol.測得CO2和CH3OH(g)的濃度隨時間變化如圖所示查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 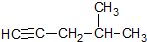 :4-甲基-1-戊炔 :4-甲基-1-戊炔 | B. | CH3CH(CH3)CH=CHCH3:2-甲基-3-戊烯 | ||
| C. | 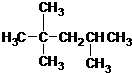 :2,2,4-三甲基戊烷 :2,2,4-三甲基戊烷 | D. |  :間二硝基苯 :間二硝基苯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| Na2O2/mol | NaHCO3/mol | 剩余固體成分 | |
| A | 1 | 2 | Na2CO3 |
| B | 1.5 | 2 | Na2O2Na2CO3 |
| C | 2 | 1 | Na2CO3、NaOH、Na2O2 |
| D | 2 | 2 | NaOH、Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室制取氣體常用的裝置如圖所示,請回答下列問題.(選用裝置時填字母編號)實驗室通常用如圖所示的裝置來制取氨氣.回答下列問題:
實驗室制取氣體常用的裝置如圖所示,請回答下列問題.(選用裝置時填字母編號)實驗室通常用如圖所示的裝置來制取氨氣.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com