
| A. |  鐵釘易被腐蝕 | |
| B. |  滴加少量KSCN溶液,溶液變為血紅色 | |
| C. | 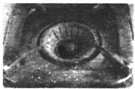 燃氣灶的中心部位容易生銹,主要是由于高溫下鐵發生化學腐蝕 | |
| D. | 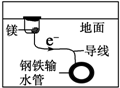 用犧牲鎂塊的方法來防止地下鋼鐵管道的腐蝕,鎂塊相當于原電池的正極 |
分析 A、鐵釘與溶液不接觸不能形成原電池,據此回答;
B、原電池鐵是負極,失去電子轉化為亞鐵離子,遇到KSCN溶液不顯色;
C、主要是由于高溫下鐵發生化學腐蝕;
D、原電池的負極金屬易生銹,可以采用犧牲陽極陰極保護法來保護金屬.
解答 解:A、鐵釘與溶液不接觸不能形成原電池,因此不易被腐蝕,故A錯誤;
B、圖2中構成原電池鐵是負極失去電子轉化為亞鐵離子,因此滴加少量KSCN溶液,溶液不會為血紅色,故B錯誤;C、燃氣灶的中心部位溫度較高,和氧氣接觸的鐵,在高溫下會發生化學反應而容易生銹,即高溫下鐵發生化學腐蝕,故C正確;
D、用犧牲鎂塊的方法來防止地下鋼鐵管道的腐蝕,鎂塊相當于原電池的負極,故D錯誤.
故選C.
點評 本題綜合考查電化學知識,側重于金屬的腐蝕與防護以及原電池的工作原理的考查,題目難度不大,注意所學知識的遷移應用.


 浙江名校名師金卷系列答案
浙江名校名師金卷系列答案 全優沖刺100分系列答案
全優沖刺100分系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 +2C2H5OH
+2C2H5OH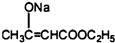 +CH3COOH→
+CH3COOH→ +CH3COONa
+CH3COONa
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某同學以甘蔗渣為原料用水解一氧化一水解循環進行制取草酸并探究測定草酸晶體(H2C2O4•xH2O)的某些性質.通過查閱資料可知:草酸易溶于水,是一種重要的化工原料,廣泛用于藥物生產、高分子合成等工業,草酸晶體受熱到100℃時失去結晶水,成為無水草酸.157℃時大量升華,并開始分解;草酸蒸氣在低溫下可冷凝為固體;草酸鈣不溶于水,草酸蒸氣能使澄清石灰水變渾濁.
某同學以甘蔗渣為原料用水解一氧化一水解循環進行制取草酸并探究測定草酸晶體(H2C2O4•xH2O)的某些性質.通過查閱資料可知:草酸易溶于水,是一種重要的化工原料,廣泛用于藥物生產、高分子合成等工業,草酸晶體受熱到100℃時失去結晶水,成為無水草酸.157℃時大量升華,并開始分解;草酸蒸氣在低溫下可冷凝為固體;草酸鈣不溶于水,草酸蒸氣能使澄清石灰水變渾濁.

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 二甲醚是一種重要的清潔燃料,也可替代氟利昂作制冷劑等,對臭氧層無破壞作用.工業上可利用煤的氣化產物(水煤氣)合成二甲醚.請回答下列問題:
二甲醚是一種重要的清潔燃料,也可替代氟利昂作制冷劑等,對臭氧層無破壞作用.工業上可利用煤的氣化產物(水煤氣)合成二甲醚.請回答下列問題:| 物質 | CH3OH | CH3OCH3 | H2O |
| 濃度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 八角茴香含有一種抗亞洲禽流感病毒的重要成分-莽草酸,其分子結構如圖所示.下列關于莽草酸的說法錯誤的是( )
八角茴香含有一種抗亞洲禽流感病毒的重要成分-莽草酸,其分子結構如圖所示.下列關于莽草酸的說法錯誤的是( )| A. | 能溶于水 | B. | 能使酸性高錳酸鉀溶液褪色 | ||
| C. | 能發生酯化反應 | D. | 遇FeCl3溶液呈紫色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 Cl2和H2O2是高中階段最常見的兩種氧化劑,經查閱資料Cl2氧化能力強于H2O2,能將H2O2氧化.為了驗證該結論,學生設計了如圖所示的實驗裝置進行實驗(夾持裝置略去).請回答下列問題:
Cl2和H2O2是高中階段最常見的兩種氧化劑,經查閱資料Cl2氧化能力強于H2O2,能將H2O2氧化.為了驗證該結論,學生設計了如圖所示的實驗裝置進行實驗(夾持裝置略去).請回答下列問題: HCl+HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.(用方程式回答).對于質疑可以采用對比實驗解決.
HCl+HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.(用方程式回答).對于質疑可以采用對比實驗解決.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com