
| A. | 一定是2L K2SO4溶液和1L Al2(SO4)3溶液混合,再加1L蒸餾水 | |
| B. | 三種液體體積比為V1:V2:V3=2:1:1 | |
| C. | 混合液中K+濃度與Al3+濃度數值之和大于SO42-濃度數值 | |
| D. | 混合液中K2SO4 物質的量等于Al2(SO4)3物質的量的一半 |
分析 c(K+)=$\frac{0.2mol/L×{V}_{1}L}{{V}_{總}}$=$\frac{0.2{V}_{1}}{{V}_{總}}$mol/L ①
(Al3+)=$\frac{0.4mol/L×{V}_{2}L}{{V}_{總}L}$=$\frac{0.4{V}_{2}}{{V}_{總}}$mol/L ②
(SO42-)=$\frac{0.1mol/L×{V}_{1}L+0.6mol/L×{V}_{2}L}{{V}_{總}L}$=$\frac{0.1{V}_{1}+0.6{V}_{2}}{{V}_{總}}$mol/L ③
將$\frac{①}{②}$可求出$\frac{{V}_{1}}{{V}_{2}}$;
從而求出V總,即可求出V1:V2:V3.
據此分析.
解答 解:c(K+)=$\frac{0.2mol/L×{V}_{1}L}{{V}_{總}}$=$\frac{0.2{V}_{1}}{{V}_{總}}$mol/L ①
(Al3+)=$\frac{0.4mol/L×{V}_{2}L}{{V}_{總}L}$=$\frac{0.4{V}_{2}}{{V}_{總}}$mol/L ②
(SO42-)=$\frac{0.1mol/L×{V}_{1}L+0.6mol/L×{V}_{2}L}{{V}_{總}L}$=$\frac{0.1{V}_{1}+0.6{V}_{2}}{{V}_{總}}$mol/L ③
將$\frac{①}{②}$可求出$\frac{{V}_{1}}{{V}_{2}}$=2:1.
設V1=2L,則V2=1L,帶入③可得V總=4L,故V3=1L.即三種液體體積比為V1:V2:V3=2:1:1.
A、三種液體體積比為V1:V2:V3=2:1:1,故混合溶液可以是2L K2SO4溶液和1L Al2(SO4)3溶液混合,再加1L蒸餾水,但不一定,故A錯誤;
B、三種液體體積比為V1:V2:V3=2:1:1,故B正確;
C、由于混合液中三種離子物質的量濃度分別為:K+:0.1mol/L,Al3+:0.1mol/L,SO42-:0.2mol/L,故K+濃度與Al3+濃度數值之和等于SO42-濃度數值,故C錯誤;
D、混合液中K2SO4 物質的量與Al2(SO4)3的物質的量之比為:$\frac{0.1mol/L×2L}{0.2mol/L×1L}$=1:1,故兩者的物質的量相等,故D錯誤.
故選B.
點評 本題考查了溶液混合后的有關計算,綜合性較強,難度適中,注意解題方法的掌握.


科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2 L乙醇所含分子數為0.5NA | |
| B. | 40 g氫氧化鈉含有氧原子數為NA | |
| C. | 1mol任何純凈物都含有6.02×1023個原子 | |
| D. | 標準狀況下,22.4 L氫氣含有NA個氫原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
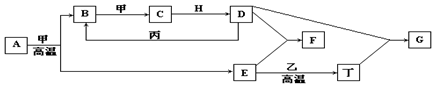
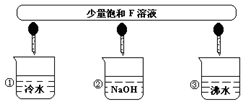
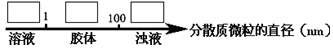
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在0℃、1.01×105Pa的條件下,某氣體的體積約為2.24×10-2m3,該氣體的物質的量為1 mol | |
| B. | 標準狀況下,相同體積的任何氣體單質所含的原子數相同 | |
| C. | 在20℃的溫度下,1 mol某氣體的體積約為22.4 L,該氣體的壓強為101 kPa | |
| D. | 固態的二氧化碳又叫干冰,含CO21 mol的干冰在標準狀況下的體積必定小于22.4 L |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 28 | B. | 36 | C. | 64 | D. | 48 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com