
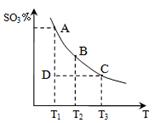
 2SO3(g)的△H____0(填“>”或“<”),若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(填“向左”、“向右”或“不移動”);
2SO3(g)的△H____0(填“>”或“<”),若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(填“向左”、“向右”或“不移動”); 2CO2+N2。它的優(yōu)點是 ;
2CO2+N2。它的優(yōu)點是 ;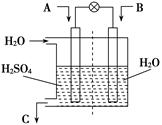


科目:高中化學 來源:不詳 題型:問答題
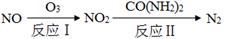
 SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1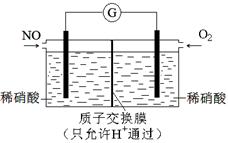
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2Z,達到平衡時,若它們的物質的量滿足:n(X)+n(Y)=n(Z),則Y的轉化率為 ( )
2Z,達到平衡時,若它們的物質的量滿足:n(X)+n(Y)=n(Z),則Y的轉化率為 ( )A.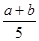 ×100% ×100% | B.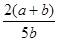 ×100% ×100% | C.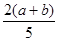 ×100% ×100% | D.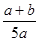 ×100% ×100% |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
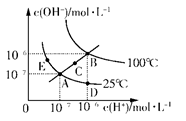
| A.圖中五點KW間的關系:B>C>A=D=E |
| B.若從A點到D點,可采用在水中加入少量酸的方法 |
| C.若從A點到C點,可采用溫度不變時在水中加入適量NaOH固體的方法 |
| D.若處在B點時,將pH=2的硫酸與pH=12的KOH等體積混合后,溶液顯中性 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
 CO2(g)+H2(g) ΔH=Q,其平衡常數(shù)隨溫度變化如下表所示:
CO2(g)+H2(g) ΔH=Q,其平衡常數(shù)隨溫度變化如下表所示:| 溫度/℃ | 400 | 500 | 850 |
| 平衡常數(shù) | 9.94 | 9 | 1 |
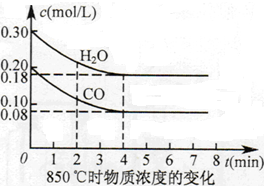
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
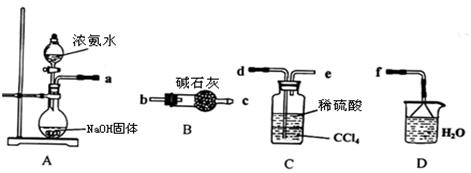
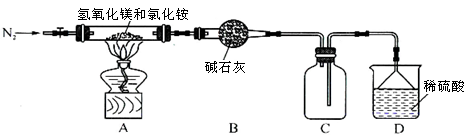
查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
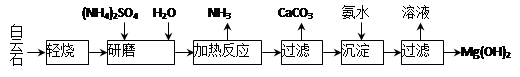
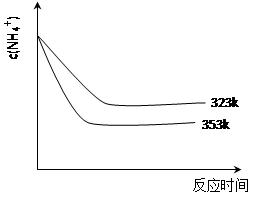
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 N2O3 + O2,N2O3
N2O3 + O2,N2O3 N2O + O2。在1L密閉容器中加熱4molN2O5,達到平衡時,c(O2)為4.5mol?L-1,c(N2O3) 為1.62mol?L-1,則c(N2O5) 為( )
N2O + O2。在1L密閉容器中加熱4molN2O5,達到平衡時,c(O2)為4.5mol?L-1,c(N2O3) 為1.62mol?L-1,則c(N2O5) 為( ) | A.1.44mol?L-1 | B.3.48mol?L-1 | C.0.94mol?L-1 | D.1.98mol?L-1 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com