
| A. | 1.1mol/L | B. | 1.5mol/L | C. | 1.2mol/L | D. | 1.0mol/L |
分析 已知:還原性強弱:I->Fe2+,所以氯氣先氧化碘離子,再氧化亞鐵離子,根據離子方程式計算.
解答 解:已知:還原性強弱:I->Fe2+,往100mL碘化亞鐵溶液中緩慢通入3.36L(標準狀況)氯氣,氯氣先氧化碘離子,再氧化亞鐵離子,已知氯氣的物質的量為$\frac{3.36L}{22.4L/mol}$=0.15mol,發生反應離子方程式為:Cl2+2I-=2Cl-+I2,碘離子完全氧化后,溶液中有$\frac{1}{2}$的Fe2+被氧化成Fe3+,發生反應離子方程式為:
Cl2+2Fe2+=2Cl-+2Fe3+,設原碘化亞鐵溶液的物質的量濃度為cmol/L,則c(I-)=2c(FeI2)=2c,c(Fe2+)=cmol/L,
所以與碘離子反應消耗的氯氣為n(Cl2)=$\frac{1}{2}$n(I-)=$\frac{1}{2}$cV=0.1cmol,
反應完成后溶液中有$\frac{1}{2}$的Fe2+被氧化成Fe3+,則與亞鐵離子反應消耗的氯氣為n(Cl2)=$\frac{1}{2}$×$\frac{1}{2}$n(Fe2+)=$\frac{1}{4}$cV=0.025cmol,所以0.025cmol+0.1cmol=0.15mol
解得:c=1.2mol/L,
故選C.
點評 本題主要考查學生氧化還原反應的有關計算,注意溶液中離子反應的順序,根據離子方程式計算,難度不大.


 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源: 題型:選擇題
| A. | CO2通入澄清石灰水中 | B. | 稀硝酸中加入銅片 | ||
| C. | 稀硝酸中加入鐵屑 | D. | HCl溶液滴入Na2CO3溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2 L苯中含有的碳碳雙鍵數目為1.5NA | |
| B. | 25℃時,1.0 L pH=12的Na2 CO3溶液中含有的陰離子數大于0.01NA | |
| C. | 標準狀況下,2.8 g由N2和CO組成的混合氣體中含有的原子數為0.1NA | |
| D. | 在反應:Cu2S+O2$\frac{\underline{\;高溫\;}}{\;}$2Cu+SO2中,生成1 mol Cu,轉移的電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
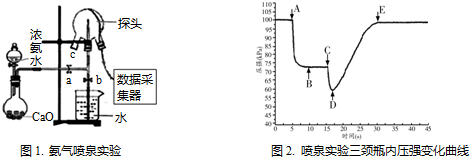
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 需鑒別物質 | 方法1 | 方法2 | |
| A | 硫酸銨和磷礦粉 | 加水溶解 | 加熟石灰 |
| B | 一氧化碳和二氧化碳 | 聞氣味 | 通過灼熱的氧化銅 |
| C | 食鹽水和蒸餾水 | 測pH | 蒸發結晶 |
| D | 真黃金和假黃金 (銅鋁合金) | 看顏色 | 灼燒 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
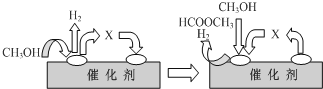
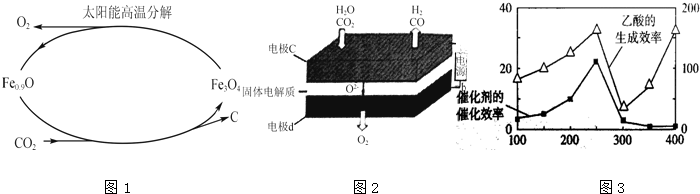
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(CH3COO-):③>① | |
| B. | 水電離出的c(OH-):②>① | |
| C. | ①和②等體積混合后的溶液:c(OH-)=c(H+)+c(CH3COOH) | |
| D. | ①和③等體積混合后的溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com