
| A. | 單質熔點:Z>W | B. | 離子半徑:X<Y | ||
| C. | 氧化物對應水化物的酸性:X>Z | D. | X和Z可存在于同一離子化合物中 |
分析 在周期表中X與Y、Z、W緊密相鄰,X、Y的原子序數之和等于Z的原子序數,所以X和Z屬于同一主族且Z在X的下一周期,原子序數不大于18,設X的原子序數是a,則a+a+1=a+8,得a=7,或a-1+a=a+8,得a=9.若a=7,則X是N,Y是O,Z是P,又X、Y、Z、W四種短周期元素原子的最外層電子數之和為20,所以W是C,符合題意.
若a=9,則X是F,Y是O,Z是Cl,三種元素原子的最外層電子數之和為20,不合題意,以此解答該題.
解答 解:在周期表中X與Y、Z、W緊密相鄰,X、Y的原子序數之和等于Z的原子序數,所以X和Z屬于同一主族且Z在X的下一周期,原子序數不大于18,設X的原子序數是a,則a+a+1=a+8,得a=7,或a-1+a=a+8,得a=9.若a=7,則X是N,Y是O,Z是P,又X、Y、Z、W四種短周期元素原子的最外層電子數之和為20,所以W是C,符合題意.若a=9,則X是F,Y是O,Z是Cl,三種元素原子的最外層電子數之和為20,不合題意;
所以X、Y、Z、W分別是N、O、P、C元素,
A.W如為金剛石,則熔點較高,故A錯誤;
B.X<Y對應的離子具有相同的核外電子排布,核電荷數越大離子半徑越小,故B錯誤;
C.非金屬性N>P,元素的非進行性越強,對應的最高價氧化物的酸性越強,但如不是最高價,則酸性強弱不一定,故C錯誤;
D.X和Z可存在于磷酸銨中,故D正確.
故選D.
點評 本題考查原子結構和元素周期律關系,側重考查分析、推斷能力,涉及物質結構、基本概念、元素周期律,正確推斷元素是解本題關鍵,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
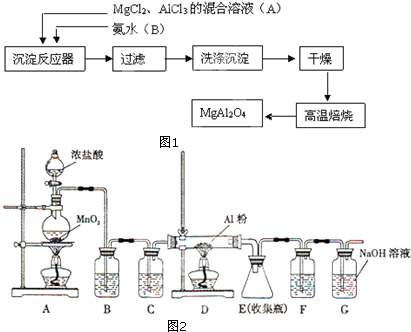
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用淀粉溶液檢驗溶液中是否存在碘離子 | |
| B. | 用分液漏斗分離水與乙醇的混合物 | |
| C. | 用氯化鋇溶液鑒別碳酸鈉溶液與硫酸鈉溶液 | |
| D. | 用排飽和食鹽水集氣法收集氯氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| t/s | 0 | 5 | 15 | 25 | 35 |
| N(M)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 35s時,N的濃度為0.80mol•L-1 | |
| B. | 達到平衡時,M的轉化率為80% | |
| C. | 相同溫度下若起始時向容器中充入1.0molP,則達到平衡時P的濃度為0.1mol•L-1 | |
| D. | 相同溫度下,起始時向容器中充入0.20molM、0.20molN和1.0molP,反應達到平衡前v(逆)<v(正) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
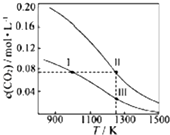 在體積均為1.0L的恒容密閉容器中加入足量的相同的碳粉,再分別加入0.1molCO2和0.2molCO2,在不同溫度下反應CO2(g)+C(s)?2CO(g)達到平衡,平衡時CO2的物質的量濃度c(CO2)隨溫度的變化如圖所示(圖中Ⅰ、Ⅱ、Ⅲ點均處于曲線上).下列說法正確的是( )
在體積均為1.0L的恒容密閉容器中加入足量的相同的碳粉,再分別加入0.1molCO2和0.2molCO2,在不同溫度下反應CO2(g)+C(s)?2CO(g)達到平衡,平衡時CO2的物質的量濃度c(CO2)隨溫度的變化如圖所示(圖中Ⅰ、Ⅱ、Ⅲ點均處于曲線上).下列說法正確的是( )| A. | 反應CO2(g)+C(s)?2CO(g)的△S>0、△H<0 | |
| B. | 體系的總壓強P總:P總(狀態Ⅱ)<2P總(狀態Ⅰ) | |
| C. | 體系中c(CO):c(CO,狀態Ⅱ)<2c(CO,狀態Ⅲ) | |
| D. | 逆反應速率V逆:V逆(狀態Ⅰ)>V逆(狀態Ⅲ) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
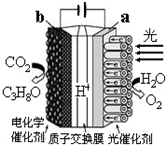 某模擬“人工樹葉”電化學實驗裝置如圖所示,該裝置能將H2O和CO2轉化為O2和C3H8O.下列說法錯誤的是( )
某模擬“人工樹葉”電化學實驗裝置如圖所示,該裝置能將H2O和CO2轉化為O2和C3H8O.下列說法錯誤的是( )| A. | 該裝置將光能和電能轉化為化學能 | |
| B. | 該裝置工作時,H+從a極區向b極區遷移 | |
| C. | 每還原44 g CO2,理論上可生成33.6L O2 | |
| D. | b電極的反應為:3CO2+18H++18e-═C3H8O+5H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com