
【題目】已知:①![]() +HNO3
+HNO3![]() +H2O ΔH<0;②硝基苯沸點210.9℃,蒸餾時選用空氣冷凝管。下列制取硝基苯的操作或裝置(部分夾持儀器略去),正確的是( )
+H2O ΔH<0;②硝基苯沸點210.9℃,蒸餾時選用空氣冷凝管。下列制取硝基苯的操作或裝置(部分夾持儀器略去),正確的是( )
A.配制混酸 B.水浴加熱
B.水浴加熱
C.洗滌后分液 D.蒸餾提純
D.蒸餾提純
科目:高中化學 來源: 題型:
【題目】某學習小組對人教版教材實驗“在200mL燒杯中放入20g蔗糖(C12H22O11),加入適量水,攪拌均勻,然后再加入15mL質量分數為98%濃硫酸,迅速攪拌”進行如下探究;
(1)觀察現象:蔗糖先變黃,再逐漸變黑,體積膨脹,形成疏松多孔的海綿狀黑色物質,同時聞到刺激性氣味,按壓此黑色物質時,感覺較硬,放在水中呈漂浮狀態,同學們由上述現象推測出下列結論:
①濃硫酸具有強氧化性 ②濃硫酸具有吸水性 ③濃硫酸具有脫水性④濃硫酸具有酸性 ⑤黑色物質具有強吸附性
其中依據不充分的是_________(填序號);
(2)為了驗證蔗糖與濃硫酸反應生成的氣態產物,同學們設計了如下裝置:

試回答下列問題:
①圖1的A中最好選用下列裝置_________(填編號);
②圖1的 B裝置所裝試劑是_________;D裝置中試劑的作用是_________;E裝置中發生的現象是_________;
③圖1的A裝置中使蔗糖先變黑的化學反應方程式為_________,后體積膨脹的化學方程式為:_________;
④某學生按圖2進行實驗時,發現D瓶品紅不褪色,E裝置中有氣體逸出,F裝置中酸性高錳酸鉀溶液顏色變淺,推測F裝置中酸性高錳酸鉀溶液顏色變淺的原因_________,其反應的離子方程式是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)[化學——選修5:有機化學基礎]
近來有報道,碘代化合物E與化合物H在Cr-Ni催化下可以發生偶聯反應,合成一種多官能團的化合物Y,其合成路線如下:
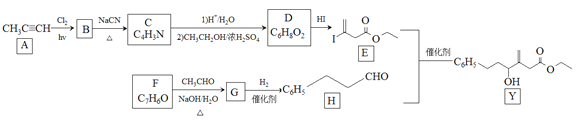
已知:![]()
回答下列問題:
(1)A的化學名稱是________________。
(2)B為單氯代烴,由B生成C的化學方程式為________________。
(3)由A生成B、G生成H的反應類型分別是________________、________________。
(4)D的結構簡式為________________。
(5)Y中含氧官能團的名稱為________________。
(6)E與F在Cr-Ni催化下也可以發生偶聯反應,產物的結構簡式為________________。
(7)X與D互為同分異構體,且具有完全相同官能團。X的核磁共振氫譜顯示三種不同化學環境的氫,其峰面積之比為3∶3∶2。寫出3種符合上述條件的X的結構簡式________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,NH3·H2O的電離平衡常數Kb=2×10-5mol·L-1,將0.5mol(NH4)2SO4溶于水中,向所得溶液中滴加aL氨水后溶液呈中性,據此判斷下列說法中不正確的是( )
A.滴加氨水的過程中,水的電離平衡將正向移動
B.滴加aL氨水后的溶液中,n(NH4+)=200n(NH3·H2O)=1mol
C.所滴加氨水的濃度為![]() mol·L-1
mol·L-1
D.滴加aL氨水后的溶液中各離子濃度大小為c(NH4+)=2c(SO42-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:25 ℃時,CH3COOH和NH3·H2O的電離常數相等。
(1)25 ℃時,取10 mL 0.1 mol·L-1醋酸溶液測得其pH=3。
①將上述(1)溶液加水稀釋至1 000 mL,溶液pH數值范圍為___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“減小”“不變”或“不能確定”)。
②25 ℃時,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH試紙測定該氨水pH的操作方法為_______________________________________________________。
③氨水(NH3·H2O溶液)電離平衡常數表達式Kb=_______________________________,25 ℃時,氨水電離平衡常數約為___________。
(2)25 ℃時,現向10 mL 0.1 mol·L-1氨水中滴加相同濃度的CH3COOH溶液,在滴加過程中c(NH4+)/c(NH3.H2O)___________(填序號)。
a.始終減小 b.始終增大 c.先減小再增大 d.先增大后減小
(3)某溫度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等濃度的醋酸溶液,溶液中pOH與pH的變化關系如圖。已知:pOH=- lgc(OH-)。

圖中M、Q、N三點所示溶液呈中性的點是___________(填字母,下同)。
圖中M、Q、N三點所示溶液中水的電離程度最大的點可能是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家研發一種低成本的鋁硫二次電池,以鋁箔和多孔碳包裹的S為電極材料,離子液體為電解液。放電時,電池反應為2Al+3S=Al2S3,電極表面發生的變化如圖所示。下列說法錯誤的是( )
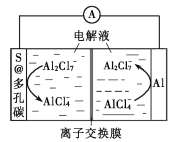
A.充電時,多孔碳電極連接電源的負極
B.充電時,陰極反應為8Al2Cl7-+6e-=2Al+14AlCl4-
C.放電時,溶液中離子的總數不變
D.放電時,正極增重0.54g,電路中通過0.06mole-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用結構和原理闡釋化學反應的類型、限度、速率和歷程是重要的化學學科思維。回答下列問題:
(1)用過氧化氫檢驗Cr(Ⅵ)的反應是Cr2O72-+4H2O2+2H+=2CrO5+5H2O。CrO5結構式為![]() ,該反應是否為氧化還原反應?___(填“是”或“否”)。
,該反應是否為氧化還原反應?___(填“是”或“否”)。
(2)已知:
2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
H2(g)+O2(g)=H2O2(l) △H=-187.8kJ·mol-1
2H2O2(l)=2H2O(l)+ O2(g) △H=___kJ·mol-1。
(3)一定條件下,H2O2分解時的c(H2O2)隨t變化如圖所示。已知該反應的瞬時速率可表示為v(H2O2)=k·cn(H2O2),k為速率常數。

①0-20min內,v(H2O2)=___。
②據圖分析,n=___。
③其它條件相同,使用活性更高的催化劑,下列說法正確的是___(填標號)。
A.v(H2O2)增大 B.k增大 C.△H減小 D.Ea(活化能)不變
(4)氣體分壓pi=p總×xi(物質的量分數)。恒溫50℃、恒壓101kPa,將足量的CuSO4·5H2O、NaHCO3置于一個密閉容器中,再充入已除去CO2的干燥空氣。假設只發生以下反應,達平衡時兩者分解的物質的量比為2:1。
CuSO4·5H2O(s)CuSO4·3H2O(s)+2H2O(g) Kp1=36(kPa)2
2NaHCO3(s)Na2CO3(s)+H2O(g)+CO2(g) Kp2
①平衡時![]() =___,Kp2=___。
=___,Kp2=___。
②平衡后,用總壓為101kPa的潮濕空氣[其中p(H2O)=8kPa、p(CO2)=0.4kPa]替換容器中的氣體,50℃下達到新平衡。容器內CuSO4·5H2O的質量將___(填“增加”“減少”或“不變”,下同),NaHCO3質量將___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應X(g)+Y(g) ![]() 2Z(g)△H<0。一定條件下,反應物Y的轉化率與反應時間的關系如圖所示。若使曲線a變為曲線b可采取的措施是
2Z(g)△H<0。一定條件下,反應物Y的轉化率與反應時間的關系如圖所示。若使曲線a變為曲線b可采取的措施是
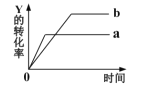
A.加入催化劑B.降低溫度C.增大壓強D.增大Y的濃度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分枝酸可用于生化研究。其結構簡式如圖。下列關于分枝酸的敘述正確的是
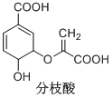
A.可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色,且原理相同
B.分子中含有4種官能團,3個手性碳原子
C.可發生消去反應,形成芳香族化合物
D.1mol分枝酸最多可與3mol NaOH發生中和反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com