
| A.當生成的沉淀量達到最大時,消耗NaOH溶液的體積V≥100 mL |
| B.當金屬全部溶解時收集到NO氣體的體積一定為2.24 L |
| C.參加反應的金屬的總質量3.6 g<m<9.6 g |
| D.當金屬全部溶解時,參加反應的硝酸的物質的量一定是0.4 mol |


科目:高中化學 來源:不詳 題型:單選題
| A.60 ml | B.45 ml. | C.30 mL | D.15mL |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 Cu2O+H2↑,則石墨應與電源的________極相連,銅電極上的電極反應式為________;電解過程中,陰極區周圍溶液pH________(填“變大”、“變小”或“不變”)。
Cu2O+H2↑,則石墨應與電源的________極相連,銅電極上的電極反應式為________;電解過程中,陰極區周圍溶液pH________(填“變大”、“變小”或“不變”)。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
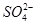 )加入足量NaOH,產生藍色沉淀,過濾,洗滌,灼燒,得到CuO 12.0 g,若上述氣體為NO和NO2的混合物,且體積比為1∶1,則V可能為
)加入足量NaOH,產生藍色沉淀,過濾,洗滌,灼燒,得到CuO 12.0 g,若上述氣體為NO和NO2的混合物,且體積比為1∶1,則V可能為| A.9.0 L | B.13.5 L | C.15.7 L | D.16.8 L |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 (NxOy)+ H2O(配平時x、y用具體數值表示,物質填在
(NxOy)+ H2O(配平時x、y用具體數值表示,物質填在 中)。
中)。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.2 mol | B.1 mol | C.0.5 mol | D.0.25 mol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.Cu與Cu2O的物質的量之比為2∶1 |
| B.硝酸的物質的量濃度為2.6 mol·L-1 |
| C.產生的NO在標準狀況下的體積為4.48 L |
| D.Cu、Cu2O與硝酸反應后剩余HNO3為0.2 mol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
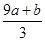 ) mol
) mol| A.①④ | B.②③ | C.①③ | D.②④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com