
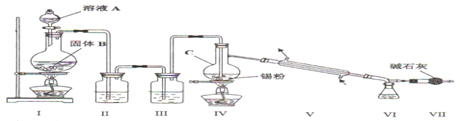
分析 由裝置圖可知裝置Ⅰ應為制備氯氣裝置,涉及離子反應為MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,裝置Ⅱ為飽和食鹽水,裝置Ⅲ為濃硫酸,氯氣經除雜,干燥后與錫在裝置Ⅳ中反應生成SnCl4,經冷卻后在裝置Ⅵ中收集,因SnCl4極易水解,應防止空氣中的水蒸氣進入裝置Ⅵ中,以此解答該題.
(1)認識常見的化學實驗儀器;
(2)A為制備氯氣裝置,在加熱條件下進行,應為濃鹽酸和二氧化錳的反應;
(3)B為飽和食鹽水,C為濃硫酸,氯氣經除雜,干燥后與錫在D中反應生成SnCl4,因SnCl4極易水解,F可起到防止空氣中的水蒸氣進入E中;、
(4)加熱促進SnCl4氣化,便于分離;
(5)若沒有III,則SnCl4會水解產生Sn(OH)4
解答 解:(1)儀器C的名稱為蒸餾燒瓶,
故答案為:蒸餾燒瓶;
(2)裝置Ⅰ中濃鹽酸與MnO2在加熱時發生反應產生氯氣.發生反應的離子方程式為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(3)由于鹽酸有揮發性,所以在制取的氯氣中含有雜質HCl,在與金屬錫反應前要除去,因此裝置Ⅱ中的最佳試劑為除去HCl同時還可以減少氯氣消耗的飽和食鹽水;SnCl4極易水解,在潮濕的空氣中發煙.為了防止鹽水解,所以要防止起水解.裝置Ⅶ的作用為防止空氣中的水蒸氣進入Ⅵ中使SnCl4水解,
故答案為:飽和氯化鈉溶液;防止空氣中水蒸氣進入Ⅵ中,SnCl4水解;
(4)加熱促進SnCl4氣化,便于分離,
故答案為:加熱促進SnCl4氣化;
(5)如果沒有裝置Ⅲ,則在氯氣中含有水蒸汽,所以在Ⅳ中除生成SnCl4外,還會生成SnCl4水解產生的含錫的化合物Sn(OH)4或SnO2,
故答案為:Sn(OH)4或SnO2等;
點評 本題考查物質的制備,涉及儀器的識別、氯氣的實驗室制取方法、實驗操作的目的、鹽的水解、物質產率的計算等知識,為高考常見題型和高頻考點,側重于學生的分析能力、實驗能力的考查,注意把握題給信息,結合物質的性質設計實驗步驟,題目難度不大.


 陽光課堂課時優化作業系列答案
陽光課堂課時優化作業系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 滴定次數 | 待測液體積(mL) | 標準鹽酸體積(mL) | |
| 滴定前讀數(mL) | 滴定后讀數(mL) | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 滴定次數 實驗數據 | 1 | 2 | 3 | 4 | 5 |
| V(NaOH)/mL(初讀數) | 0.00 | 0.20 | 0.00 | 0.10 | 0.05 |
| V(NaOH)/mL(終讀數) | 15.75 | 15.20 | 14.98 | 15.12 | 15.05 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 少量的氯水加入到盛有NaBr溶液的試管中 | |
| B. | 取一小片鋁,砂紙除去氧化膜,放入試管中,加入少量2mL水 | |
| C. | 將鋅片與銅片用導線連接,插入盛稀硫酸的燒杯中 | |
| D. | 向盛有過氧化氫水溶液的試管中,加入少量1mol/LFeCl3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
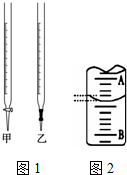 某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:
某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:| 滴定次數 | 標準鹽酸體積/mL | 待測液體積/mL | |
| 滴定前讀數 | 滴定后讀數 | ||
| 第一次 | 20.00 | 0.52 | 19.42 |
| 第二次 | 20.00 | 4.07 | 23.17 |
| 第三次 | 20.00 | 1.08 | 20.08 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10 mL 0.1 mol/L AlCl3溶液 | B. | 20 mL 0.1 mol/L CaCl2溶液 | ||
| C. | 30 mL 0.2 mol/L KCl溶液 | D. | 200 mL 2 mol•L-1KClO3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com