
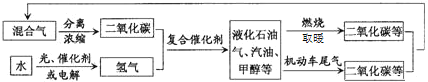
【題目】科學家正在研究建立如圖所示的二氧化碳新循環體系以解決日益加劇的溫室效應等問題,關系圖中能反映的化學觀點或化學思想有( )
①二氧化碳也是一種重要的資源;
②光能或電能可以轉化為化學能;
③燃燒時化學能可以轉化為熱能;
④無機物和有機物可以相互轉化;
⑤化學變化中元素種類是守恒的
A.①②③B.①④⑤C.①②④⑤D.①②③④⑤
【答案】D
【解析】
①從圖示中可以看出,二氧化碳和氫氣在一定條件下可以轉化為甲醇等能源,二氧化碳在很多工業和農業中有大量的應用,所以二氧化碳也是一種重要的資源,①正確;
②水在光催化劑或電解生成氫氣和氧氣,體現了光能或電能可以轉化為化學能,②正確;
③液化石油氣、汽油、甲醇等有機物的燃燒,都說明了燃燒時化學能可以轉化為熱能和光能,③正確;
④液化石油氣、汽油、甲醇轉化為二氧化碳,無機物二氧化碳和氫氣在復合催化劑的催化作用下可以轉化為甲醇等有機物,說明無機物和有機物可以相互轉化,④正確;
⑤由圖可知,混合氣分離出二氧化碳,水分解生成氫氣,二氧化碳和氫氣在一定條件下可以轉化為甲醇等能源都遵循化學變化中元素種類守恒的原則,⑤正確;
答案選D。


 黃岡海淀全程培優測試卷系列答案
黃岡海淀全程培優測試卷系列答案科目:高中化學 來源: 題型:
【題目】常溫下,用0.1000mol·L-1 NaOH溶液滴定20.00mL 0.1000 mol·L-1某酸(HA)溶液,溶液中HA、A-的物質的量分數δ(X)隨pH的變化如圖所示。[已知δ(X)=![]() ]下列說法正確的是
]下列說法正確的是
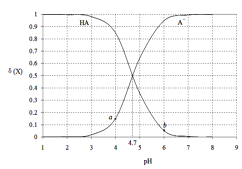
A.Ka(HA)的數量級為10-5
B.溶液中由水電離出的c(H+):a點>b點
C.當pH=4.7時,c(A-)+c(OH-)=c(HA)+c(H+)
D.當pH=7時,消耗NaOH溶液的體積為20.00mL
查看答案和解析>>
科目:高中化學 來源: 題型:
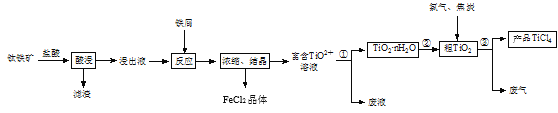
【題目】四氯化鈦(TiCl4)是制取航空材料——鈦合金的重要原料。由鈦鐵礦(主要成分是FeTiO3,不溶于水)制備TiCl4等產品的一種工藝流程示意如圖:
回答下列問題:
(1)“酸浸”時需要將鈦鐵礦粉碎,其目的是____。
(2)浸出液呈強酸性,含有TiO2+、Fe2+及少量Fe3+、Al3+等離子,則生成TiO2+的離子方程式是__。
(3)“反應”時需加入鐵屑至浸出液顯紫色,此時溶液仍呈強酸性。該過程中有如下反應發生:
2Fe3++Fe=3Fe2+
2TiO2+(無色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(無色)+Fe2++2H+
加入鐵屑的作用是____。
(4)通過控制條件,可以使過程①中生成的TiO2·nH2O形成一種液態分散系,用一束光照射該分散系能夠產生丁達爾效應,則分散質顆粒直徑的范圍是____。
(5)過程①制得的固體TiO2·nH2O需用過量酸清洗以除去其中的Fe(OH)3雜質,檢驗Fe(OH)3雜質除凈的實驗方法是____。
(6)過程③生成的廢氣中含有CO,則TiO2和焦炭、氯氣在高溫下發生反應的化學方程式是___。
(7)上述工藝具有成本低、可用低品位礦物為原料等優點。依據綠色化學理念,該工藝流程中存在的不足之處是____(只要求寫出一項)。
(8)依據表中信息,可采用___方法精制含少量SiCl4雜質的TiCl4。
TiCl4 | SiCl4 | |
熔點/℃ | -25.0 | -68.8 |
沸點/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、D、E、W是中學常見的四種元素,原子序數依次增大,A的原子最外層電子數是次外層的2倍,D的氧化物屬于兩性氧化物,D、E位于同周期,A、D、E的原子最外層電子數之和為14,W是人體必需的微量元素,缺乏W會導致貧血癥狀。
(1)W在元素周期表中的位置是___。A與E組成的化合物是常用的溶劑,寫出其電子式___。
(2)下列事實能用元素周期表相應規律解釋的是(填字母序號)___。
a.D的最高價氧化物對應水化物的堿性弱于Mg(OH)2
b.E的氣態氫化物的穩定性小于HF
c.A的單質能與二氧化硅高溫下制得粗品硅單質
(3)WE3的溶液可用于刻蝕銅制的印刷電路板,反應的離子方程式為____。
(4)①工業上用電解法制備D的單質,反應的化學方程式為___。
②家用“管道通”的有效成分是燒堿和D的單質,使用時需加入一定量的水,此時發生反應的化學方程式為____。
(5)W的單質可用于處理酸性廢水中的NO3-,使其轉換為NH4+,同時生成有磁性的W的氧化物X,再進行后續處理,上述反應的離子方程式為__。上述W的氧化物X能與D的單質反應,寫出該反應的化學方程式為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以硫鐵礦(主要成分為FeS2,還有少量CuS、SiO2等雜質)為原料制備綠礬晶體(FeSO4·7H2O)的工藝流程如下:
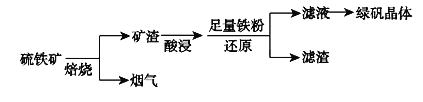
(1)煙氣中的SO2會污染環境,可用足量氨水吸收,寫出該反應的離子方程式___。
(2)檢驗濾液中金屬陽離子所用試劑及現象為____、____。
(3)FeSO4溶液制備綠礬晶體過程中要保持H2SO4過量,理由___。(結合化學用語說明原因)
(4)燃料細菌脫硫法是用氧化亞鐵硫桿菌(T.f)對硫鐵礦進行催化脫硫,同時得到FeSO4溶液。其過程如圖所示:
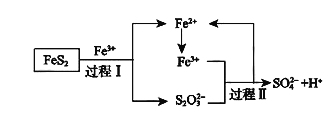
已知總反應為:FeS2+14Fe3++8H2O=2SO42-+15Fe2++16H+
①將過程I離子方程式補充完整
___FeS2+___Fe3++____=7Fe2++___S2O32-+___,__
②過程II反應的離子方程式____。
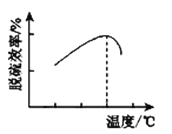
③研究發現,用氧化亞鐵硫桿菌(T.f)脫硫,溫度過高脫硫效率降低(如圖),可能的原因是___。
(5)綠礬晶體在空氣中易被氧化。取X g樣品,加水完全溶解,用酸性KMnO4標準溶液滴定,終點現象為___;酸性KMnO4 溶液氧化Fe2+ 的離子方程式:____;配制酸性高錳酸鉀溶液時下列操作將導致Fe2+的濃度偏大的是__。
a.定容時仰視 b.容量瓶洗滌后未干燥直接進行配制
c.定容搖勻后液面下降 d.未洗滌燒杯和玻璃棒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,甘氨酸在水溶液中解離情況如下: 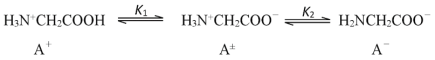 ,改變溶液pH值,三種甘氨酸相關離子的分布分數(α,平衡時某物種的濃度占各物種濃度之和的分數)變化如圖所示。當調節溶液的pH值使甘氨酸所帶的凈電荷為零,此時溶液的pH叫等電點。下列說法正確的是
,改變溶液pH值,三種甘氨酸相關離子的分布分數(α,平衡時某物種的濃度占各物種濃度之和的分數)變化如圖所示。當調節溶液的pH值使甘氨酸所帶的凈電荷為零,此時溶液的pH叫等電點。下列說法正確的是
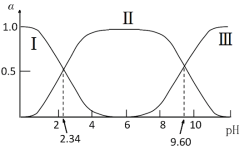
A.曲線Ⅰ、Ⅱ、Ⅲ分別代表的微粒為A-、![]() 、A+
、A+
B.K2=10-2.34,且K2對應的解離基團為—NH3+
C.在pH=9.60的溶液中加鹽酸,α(![]() )+α(A+)+α(A-)保持不變
)+α(A+)+α(A-)保持不變
D.甘氨酸的等電點pH約為6,且存在c(![]() )=c(A+)=c(A-)
)=c(A+)=c(A-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二甲醚(CH3OCH3)重整制取H2,具有無毒、無刺激性等優點。回答下列問題:
(1) CH3OCH3和O2發生反應Ⅰ: CH3OCH3(g)+![]() O2 (g) =2CO(g)+3H2(g) △H
O2 (g) =2CO(g)+3H2(g) △H
己知:CH3OCH3(g) =CO(g)+H2(g)+CH4(g) △H= a kJ/mol
CH4(g) +![]() O2 (g) = CO(g)+2H2O(g) △H= b kJ/mol
O2 (g) = CO(g)+2H2O(g) △H= b kJ/mol
H2(g)+![]() O2 (g) = H2O(g) △H= c kJ/mol
O2 (g) = H2O(g) △H= c kJ/mol
①則反應Ⅰ的△H=_________________ (用含a、b、c的代數式表示)。
②保持溫度和壓強不變,分別按不同進料比通入CH3OCH3和O2,發生反應Ⅰ。測得平衡時H2的體積百分含量與進料氣中![]() 的關系如圖(a)所示。當
的關系如圖(a)所示。當![]() >0.6時,H2的體積百分含量快速降低,其最主要原因是_____
>0.6時,H2的體積百分含量快速降低,其最主要原因是_____![]() 填標號
填標號![]() 。
。
a 過量的O2起稀釋作用
b 過量的O2與H2發生副反應生成H2O
c ![]() >0.6時平衡向逆反應方向移動
>0.6時平衡向逆反應方向移動
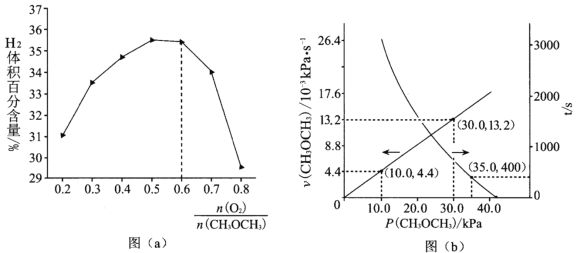
(2)T℃時,在剛性反應器中通入CH3OCH3,發生反應Ⅱ:CH3OCH3(g) =CO(g)+H2(g)+CH4(g) △H>0,測得容器內初始壓強為41.6kPa,反應過程中反應速率v(CH3OCH3)、時間t與分壓P(CH3OCH3)的關系如圖(b)所示。
①t=400s時,CH3OCH3的分解率α=______(保留2位有效數字);
②反應速率滿足v(CH3OCH3)=k Pn(CH3OCH3),n=_____,k=______s-1;400s時v(CH3OCH3)=___________kPa·s-1。
③一段時間后反應達到平衡,測得體系的總壓強為121.6 kPa,則該反應的平衡常數Kp=_____kPa2。
④若提高該剛性反應器的溫度,再次達到平衡后體系的壓強P_____121.6 kPa(填“大于”、“等于”或“小于”),原因是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖曲線a和b是可溶性一元強堿與鹽酸互滴的滴定曲線,下列說法正確的是
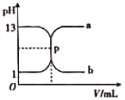
A.可溶性一元強堿、鹽酸的物質的量濃度均為1mol·L-1
B.p點為滴定終點(兩者恰好完全反應),溶液呈中性
C.酚酞不能用作該滴定的指示劑
D.曲線b是可溶性一元強堿滴定鹽酸的滴定曲線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為某原電池裝置:

(1)若A為銅,B為鐵,電解質溶液為Fe2(SO4)3溶液,則鐵片為______極(填“正”或“負”),A極電極反應式為_______,是_______(填“氧化反應”或“還原反應”)。
(2)若A為PbO2,B為Pb,電解質溶液為稀硫酸,放電時的方程式為:PbO2+Pb+2H2SO4=2PbSO4+2H2O,則B極的電極反應式為_________,H+向__________(填“正”或“負”)極移動。
(3)若A、B均為Pt電極,電解質溶液為稀硫酸,則向A極通入H2, B極通入O2,B極的反應為:O2+4e-+4H+=2H2O,則A極的電極反應式為_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com