
【題目】(1)NH3經一系列反應可以得到HNO3和NH4NO3,如圖所示,

在Ⅰ中,NH3和O2在催化劑作用下反應,其化學方程式是:__________________________

(2)Ⅱ中,2NO(g)+ O2(g) 2NO2(g).在其他條件相同時,分別測得NO的平衡轉化率在不同壓強(p1、p2)下溫度變化的曲線(如圖).
①p1、p2的大小關系p1 ________ p2(填大于、等于、小于) .
②隨溫度升高,該反應平衡常數變化的趨勢是_________________________
(3)Ⅲ中,降低溫度,將NO2(g)轉化為N2O4(1)再制備濃硝酸.
N2O4與O2, H2O化合的化學方程式是______________________________
(4)Ⅳ中,電解NO制備NH4NO3,其原理原理如下圖所示,為使電解產物全部轉化為NH4NO3, 需補充物質___________ ,說明理由:___________________.
 .
.
【答案】4NH3+5O2![]() 4NO+6H2O 小于 變小 2N2O4+O2+2H2O=4HNO3 NH3 根據反應8NO+7H2O
4NO+6H2O 小于 變小 2N2O4+O2+2H2O=4HNO3 NH3 根據反應8NO+7H2O![]() 3NH4NO3+2HNO3,電解生成的HNO3多,所以需充入NH3.
3NH4NO3+2HNO3,電解生成的HNO3多,所以需充入NH3.
【解析】
在催化劑、加熱條件下,氨氣被氧化生成NO和水;相同溫度下,增大壓強,平衡向正反應方向移動,則NO的轉化率增大;根據圖象知,相同壓強下,升高溫度,NO轉化率減小,說明正反應是放熱反應,據此判斷化學平衡常數與溫度的關系;N2O4、O2和H2O反應生成硝酸;電解NO制備NH4NO3,陽極反應為NO-3e-+2H2O=NO3-+4H+,陰極反應為:NO+5e-+6H+=NH4++H2O,根據轉移電子守恒判斷需要加入物質。
(1)氨的催化氧化的反應方程式為4NH3+5O2![]() 4NO+6H2O。(2)①由2NO(g)+O2(g)
4NO+6H2O。(2)①由2NO(g)+O2(g)![]() 2NO2(g)可知該反應為氣體體積減小的反應,溫度相同,增大壓強,平衡正向移動,NO的平衡轉化率增大,根據圖示和坐標含義,判斷p1<p2;②再看同一壓強線,溫度升高,NO的平衡轉化率降低,平衡向逆反應方向移動,則正反應為放熱反應,溫度升高,平衡常數減小。(3)N2O4、O2和H2O反應生成硝酸的反應方程式為2N2O4+ O2+2H2O=4HNO3。(4)根據工作原理裝置圖,可以確定陽極為NO失去電子轉變為NO3—,陰極NO轉變為NH4+,根據電極反應書寫電極反應式為:陽極:NO-3e-+2H2O= NO3—+4H+,陰極:NO+5e-+ 6H+= NH4++ H2O,然后根據得失電子守恒,硝酸根離子物質的量比銨根離子物質的量多,所以需要向溶液中加入的物質為NH3(即8NO+7H2O=3NH4NO3+2HNO3)。
2NO2(g)可知該反應為氣體體積減小的反應,溫度相同,增大壓強,平衡正向移動,NO的平衡轉化率增大,根據圖示和坐標含義,判斷p1<p2;②再看同一壓強線,溫度升高,NO的平衡轉化率降低,平衡向逆反應方向移動,則正反應為放熱反應,溫度升高,平衡常數減小。(3)N2O4、O2和H2O反應生成硝酸的反應方程式為2N2O4+ O2+2H2O=4HNO3。(4)根據工作原理裝置圖,可以確定陽極為NO失去電子轉變為NO3—,陰極NO轉變為NH4+,根據電極反應書寫電極反應式為:陽極:NO-3e-+2H2O= NO3—+4H+,陰極:NO+5e-+ 6H+= NH4++ H2O,然后根據得失電子守恒,硝酸根離子物質的量比銨根離子物質的量多,所以需要向溶液中加入的物質為NH3(即8NO+7H2O=3NH4NO3+2HNO3)。


 手拉手全優練考卷系列答案
手拉手全優練考卷系列答案科目:高中化學 來源: 題型:
【題目】一定溫度下,向飽和苛性鈉溶液中放一定量的過氧化鈉,充分反應后恢復到原溫度,下列有關說法中,正確的是
A.溶液中Na+濃度增大,有O2放出B.溶液pH不變,有H2放出
C.溶液中Na+數目減少,有O2放出D.溶液中pH增大,有O2放出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】原電池是化學對人類的一項重大貢獻。
(1)某興趣小組為研究電池原理,設計如圖A裝置。
|
|
A | B |
①a和b不連接時,燒杯中發生反應的離子方程式是___________________。
②a和b用導線連接,Cu極為原電池________(填“正”或“負”)極,該電極反應式是____________________________。
③無論a和b是否連接,Zn片均被腐蝕,若轉移了0.4 mol電子,則理論上Zn片質量減輕________ g。
(2)如圖B是甲烷燃料電池原理示意圖,回答下列問題:
①電池的負極是________(填“a”或“b”)電極,該極的電極反應式為________________。
②電池工作一段時間后電解質溶液的pH________(填“增大”“減小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“保護地球,人人有責”。開發新能源,倡導低碳經濟對環境保護有重要的意義與作用。下列說法不正確的是( )
A.CO2、甲烷都屬于溫室氣體
B.太陽能、風能和生物能均屬于新能源
C.太陽能電池可將太陽能直接轉化為電能
D.用甘蔗生產的乙醇燃料屬于可再生能源,利用乙醇燃料不會產生溫室氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸鈷可用于指示劑和催化劑的制備。用水鈷礦(主要成分為Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工藝流程如下:
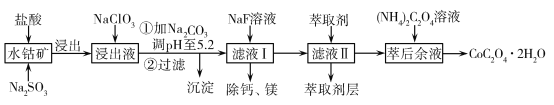
已知:①浸出液含有的陽離子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性條件下,ClO不會氧化Co2+,ClO轉化為Cl-;③部分陽離子以氫氧化物形式沉淀時溶液的pH見表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)浸出過程中加入Na2SO3的主要目的是________。
(2)向浸出液中加入NaClO3的離子反應方程式:________。
(3)已知:常溫下NH3·H2O![]() NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5
H2C2O4![]() H++HC2O4- Ka1=5.4×10-2 HC2O4-
H++HC2O4- Ka1=5.4×10-2 HC2O4-![]() H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5
則該流程中所用(NH4)2C2O4溶液的pH________7(填“>”或“<”或“=”)。
(4)加入(NH4)2C2O4 溶液后析出晶體,再過濾、洗滌,洗滌時可選用的試劑有:________。
A.蒸餾水 B.自來水
C.飽和的(NH4)2C2O4溶液 D.稀鹽酸
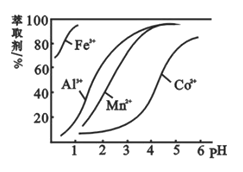
(5)萃取劑對金屬離子的萃取率與pH的關系如圖,萃取劑的作用是________;其使用的適宜pH范圍是________。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的數值,下列說法不正確的是
A. 23g Na與O2充分反應生成Na2O和Na2O2的混合物,消耗O2的分子數N(O2)的范圍為:0.25 NA< N(O2)< 0.5 NA
B. 2 mol NO和1 mol O2在密閉容器中充分反應,反應后容器中的分子數小于2NA
C. 2.5gMg-Zn合金與足量鹽酸反應,放出的氣體在標況下的體積可能為2.24L
D. 50 mL 18.4 mol/L濃硫酸與足量銅微熱反應,轉移的電子數目為0.92NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聚合物H ( )是一種聚酰胺纖維,廣泛用于各種剎車片,其合成路線如下:
)是一種聚酰胺纖維,廣泛用于各種剎車片,其合成路線如下:

已知:①C、D、G均為芳香族化合物,分子中均只含兩種不同化學環境的氫原子。
②Diels-Alder反應:![]() 。
。
(1)生成A的反應類型是_______。D的名稱是_______。F中所含官能團的名稱是_______。
(2)B的結構簡式是_______;“B→C”的反應中,除C外,另外一種產物是_______。
(3)D+G→H的化學方程式是______。
(4)Q是D的同系物,相對分子質量比D大14,則Q可能的結構有______種,其中核磁共振氫譜有4組峰,且峰面積比為1:2:2:3的結構簡式為______(任寫一種)。
(5)已知:乙炔與1,3-丁二烯也能發生Diels-Alder反應。請以1,3-丁二烯和乙炔為原料,選用必要的無機試劑合成 ,寫出合成路線__________(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)。
,寫出合成路線__________(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖中表示碳原子相互結合的幾種方式。小圓球表示碳原子,小棍表示化學鍵,假如碳原子上其余的化學鍵都是與氫原子結合,則下列說法正確的是
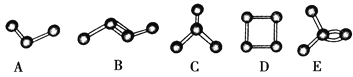
A. 圖中屬于烷烴的是A、C、D
B. 圖中C和E分子中氫原子數相同
C. 圖中物質碳元素的質量分數最小的是A
D. 圖中與B互為同分異構體的有C、D、E
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸是基礎化工的重要產品,工業上制備硫酸的主要反應為:
造氣: 4 FeS2 +11O2 ![]() 2 Fe2O3+ 8 SO2
2 Fe2O3+ 8 SO2
催化氧化: 2 SO2 + O2 ![]() 2 SO3
2 SO3
吸收: SO3 + H2O → H2SO4
完成下列填空:
(1)一定條件下,1 mol SO2和0.75 mol O2在容積為1 L的恒容密閉容器中發生反應,5 min時達到化學平衡。
①反應達到平衡后若改變條件使平衡常數K值變大,則在平衡移動過程中υ(正) _______(填序號)
a.一直增大 b.一直減小 c.先增大后減小 d.先減小后增大
②達到平衡時若SO3的濃度為0.98 mol·L-1,則5min內氧氣的反應速率為_________ mol·L-1·min-1。反應體系中氧氣過量的目的是_____________________。
(2)催化氧化反應中,SO2的平衡轉化率與溫度、壓強的關系如圖所示。則工業生產中最適宜的壓強為___________,最適宜的溫度范圍為___________。

(3)若制取硫酸的上述三個反應過程中硫元素的轉化率都是98%, 則1 mol硫鐵礦可以制得SO2____________L(標準狀況下),最終得到純硫酸______________mol(均保留2位小數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com