
| 實驗步驟 | 預期現象和結論 |
| 取少量反應后的混合溶液分別置于A、B兩試管中:往A中滴加KSCN溶液;往B中滴加淀粉溶液 | ①A中溶液變紅,B中溶液不變藍, 則假設1成立. ②A中溶液不變紅,B中溶液變藍, 則假設2成立. |
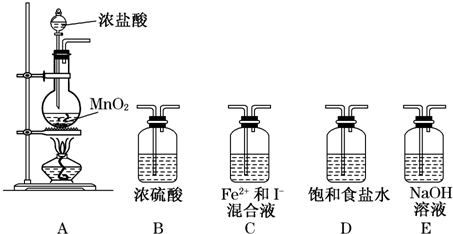
分析 (1)依據實驗的目的“將少量Cl2通入Fe2+和I-的混合溶液中,探究Fe2+和I-的還原性強弱”解答,有毒氣體要進行尾氣處理;
(2)三價鐵離子遇到KSCN溶液顯紅色,淀粉遇到碘變藍色,當通入少量的氯氣時,如果二價鐵離子先反應被氧化物三價鐵離子,則加入KSCN溶液顯紅色,
碘離子此時未反應,加入淀粉后不變藍色;如果碘離子先反應被氧化為單質碘,則加入淀粉變藍色,二價鐵離子此時未反應,加入KSCN溶液不變紅色;
(3)依據2Fe2++Cl2=2Fe3++2Cl-計算1.52g FeSO4固體中二價鐵離子被氧化需要的氯氣的物質的量,依據2I-+Cl2=I2+2Cl-,計算1.66g KI固體被氧化需要的氯氣的物質的量;
(4)依據氧化還原反應中還原劑的還原性大于還原產物的還原性來判斷.
解答 解:(1)要想探究Fe2+和I-的還原性強弱,應將制取的氯氣通入到含有Fe2+和I-的溶液中,氯氣有毒應進行尾氣處理,即最后需要通過NaOH溶液吸收多余的氯氣,所以必須的裝置A→C→E,
故答案為:C→E;
(2)三價鐵離子遇到KSCN溶液顯紅色,淀粉遇到碘變藍色,當通入少量的氯氣時,如果二價鐵離子先反應被氧化物三價鐵離子,則加入KSCN溶液顯紅色,
碘離子此時為反應,加入淀粉后不變藍色;如果碘離子先反應被氧化為單質碘,則加入淀粉變藍色,二價鐵離子此時未反應,加入KSCN溶液不變紅色;
若滴加KSCN溶液變紅色,滴加淀粉變藍色,則說明Fe2+和I-都被氧化,二者一樣強;
故答案為:
| 實驗步驟 | 預期現象和結論 |
| ①A中溶液變紅,B中溶液不變藍, ②A中溶液不變紅,B中溶液變藍. |
點評 本題考查了實驗方案設計和鐵的化合物的性質,題目難度中等,側重于考查學生的實驗探究能力和對基礎知識的應用能力,明確反應的實質和氧化還原反應的先后規律是解題的關鍵.


 輕松奪冠全能掌控卷系列答案
輕松奪冠全能掌控卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 第Ⅰ組 | 第Ⅱ組 | 第Ⅲ組 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Fe | NaOH | MgCl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③⑤⑥ | B. | ②③④⑥ | C. | ①②④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 該裝置為原電池 | |
| B. | a極上發生還原反應 | |
| C. | 電子由b→a | |
| D. | 該過程中能量的轉換只有化學能與電能的轉化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1-丙醇與濃氫溴酸反應:CH3CH2 CH2OH+HBr$\stackrel{△}{→}$CH3CH2 CH2Br+H2O | |
| B. | 1-溴丙烷與氫氧化鈉溶液共熱:CH3CH2 CH2Br+NaOH$→_{△}^{水}$CH3CH2 CH2OH+NaBr | |
| C. | 苯酚鈉中通入少量二氧化碳:2 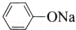 +CO2+H2O→2 +CO2+H2O→2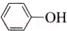 +Na2CO3 +Na2CO3 | |
| D. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硫酸}$C6H12O6(果糖)+C6H12O6(葡萄糖) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 20:1 | B. | 1:20 | C. | 10:1 | D. | 1:10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| 選項 | 現象 | 結論 |
| A | ①中導管口冒氣泡,手松開無現象 | 氣密性良 |
| B | ②中KMnO4溶液紫紅色褪去 | SO2具有漂白性 |
| C | ③中關閉K,氣體顏色在熱水中比冷水深 | NO2生成N2O4為吸熱反應 |
| D | ④中燒瓶中形成噴泉 | Cl2易溶于CCl4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com