
| A. | 碳酸鈣受熱分解 | B. | 天然氣的燃燒 | ||
| C. | 鋁粉與稀鹽酸反應 | D. | 生石灰變成熟石灰 |
分析 根據常見的放熱反應有:所有的物質燃燒、所有金屬與酸反應、金屬與水反應,所有中和反應、絕大多數化合反應和鋁熱反應;
常見的吸熱反應有:絕大數分解反應,個別的化合反應(如C和CO2),少數分解置換以及某些復分解(如銨鹽和強堿).
解答 解:A、碳酸鈣在高溫下的分解反應是吸熱反應,故A正確;
B、天然氣的燃燒反應放出大量的熱,則屬于放熱反應,故B錯誤;
C、金屬與酸的反應,屬于放熱反應,故C錯誤;
D、生石灰和水發生反應生成熟石灰,屬于化合反應,為放熱反應,故D錯誤.
故選A.
點評 本題考查吸熱反應,抓住中學化學中常見的吸熱或放熱的反應是解題的關鍵,對于特殊過程中的熱量變化的要熟練記憶來解答此類習題.


科目:高中化學 來源: 題型:解答題
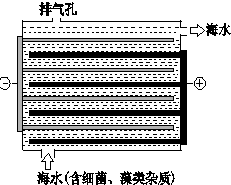 海洋化學資源的研究和合理利用具有廣闊前景,從海水中可提取氯、溴、碘等鹵族元素.
海洋化學資源的研究和合理利用具有廣闊前景,從海水中可提取氯、溴、碘等鹵族元素.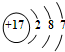 ,碘在元素周期表中的位置是第五周期ⅦA族,HI的穩定性比HBr弱(填寫“強”或“弱”).
,碘在元素周期表中的位置是第五周期ⅦA族,HI的穩定性比HBr弱(填寫“強”或“弱”).| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在標準狀況下,NA個水分子所占的體積約為22.4L | |
| B. | 5.6g鐵與氯氣完全反應,失去電子的數目為0.2NA | |
| C. | 1mol C12發生化學反應,轉移的電子數一定為2NA | |
| D. | 在標準狀況下,22.4L由N2、N2O組成的混合氣體中所含有的氮原子為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵片粉與稀硝酸反應:Fe+2H+═Fe2++H2↑ | |
| B. | 氧化亞鐵粉末溶于鹽酸中:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 銅與氯化鐵溶液反應:2Fe3++Cu═2Fe2++Cu2+ | |
| D. | 向硫酸鋁溶液中加入過量氨水:Al3++4OH-═AlO2+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②⑤ | B. | ①③⑤ | C. | ①③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
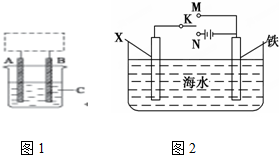 (I)研究CO2的利用對促進低碳社會的構建具有重要的意義.將CO2與焦炭作用生成CO,CO可用于煉鐵等.
(I)研究CO2的利用對促進低碳社會的構建具有重要的意義.將CO2與焦炭作用生成CO,CO可用于煉鐵等.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com