
 ; Z在周期表中的位置是第三周期ⅥA族;B元素的名稱為碳.
; Z在周期表中的位置是第三周期ⅥA族;B元素的名稱為碳.分析 常見的10電子化合物有CH4、NH3、H2O、HF等,多為氫化物,A與B和A與X均可形成10個電子化合物,則A為H元素,常見化合物Y2X2與水反應生成X的單質,其溶液可使酚酞試液變紅,則該化合物為Na2O2,其中Y為Na元素,X為O元素,X與Z同主族,則Z為S元素,最外層電子數為6,B與Z的最外層電子數之比為2:3,則B的最外層電子數為4,根據A、B、X、Y和Z是原子序數依次遞增可知B為C元素,根據元素所在周期表中的位置,原子結構以及對應化合物的性質解答該題.
解答 解:常見的10電子化合物有CH4、NH3、H2O、HF等,多為氫化物,A與B和A與X均可形成10個電子化合物,則A為H元素,常見化合物Y2X2與水反應生成X的單質,其溶液可使酚酞試液變紅,則該化合物為Na2O2,其中Y為Na元素,X為O元素,X與Z同主族,則Z為S元素,最外層電子數為6,B與Z的最外層電子數之比為2:3,則B的最外層電子數為4,根據A、B、X、Y和Z是原子序數依次遞增可知B為C元素,
(1)Y為Na元素,鈉離子的核電荷數為11,核外電子總數為10,其離子結構示意圖為: ;Z為S元素,原子核外有3個電子層,最外層電子數為6,位于周期表第三周期ⅥA族;B為C元素,名稱為碳,
;Z為S元素,原子核外有3個電子層,最外層電子數為6,位于周期表第三周期ⅥA族;B為C元素,名稱為碳,
故答案為: ;第三周期ⅥA族;碳;
;第三周期ⅥA族;碳;
(2)化合物Y2X2為Na2O2,其電子式為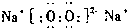 ,屬于離子化合物,故A正確,
,屬于離子化合物,故A正確,
故答案為:A;
(3)A與X和A與Z形成的18電子化合物分別為H2O2、H2S,其中H2O2具有氧化性,H2S具有還原性,二者發生氧化還原反應生成S和H2O,反應的化學方程式為:H2O2+H2S=S↓+2H2O,
故答案為:H2O2+H2S=S↓+2H2O;
(4)堿性氫氧燃料電池中,通入氫氣的一極為電源的負極,通入氧氣的一極為電源的正極;氫氧根離子帶負電荷,其移動方向與電流方向相反,電解質溶液中,電流從負極流向正極,則氫氧根離子向負極移動,
故答案為:氧氣;負;
(5)①光解海水,可充分利用光能,廉價而又低碳,符合要求,故①正確;
②鋅和稀硫酸反應,消耗大量的鋅和硫酸,不符合廉價的要求,故②錯誤;
故答案為:①.
點評 本題考查元素位置結構性質的關系及應用,題目難度中等,本題側重于物質的結構和性質的考查,學習中注重相關基礎知識的積累,試題培養了學生的分析、理解能力及靈活應用基礎知識的能力.


科目:高中化學 來源: 題型:選擇題
 轉變為
轉變為 的方法為( )
的方法為( )| A. | 與足量NaOH溶液共熱后,再通入CO2 | |
| B. | 與稀H2SO4共熱后,加入足量Na2CO3 | |
| C. | 與稀H2SO4共熱后,加入足量NaOH | |
| D. | 與足量NaOH溶液共熱后,再加入稀硫酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl的電子式H:Cl | B. | HClO的結構式:H-Cl-O | ||
| C. | Cl-的結構示意圖: | D. | 質量數為37的氯原子:37Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2的電子式: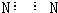 | B. | S2-的結構示意圖: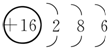 | ||
| C. | 次氯酸的結構式:H-O-Cl | D. | ${\;}_{40}^{65}$Zr和${\;}_{40}^{67}$Zr是同種核素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{53}^{131}$I元素中含中子數為53 | |
| B. | 它是碘元素的一種同位素 | |
| C. | ${\;}_{53}^{131}$I2的摩爾質量為262 g | |
| D. | 由此可確定碘元素相對原子質量為131 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在氧化還原反應中,甲比乙失電子多 | |
| B. | 同價態的陽離子,甲比乙氧化性強 | |
| C. | 甲能與稀硫酸反應生成氫氣而乙不能 | |
| D. | 甲的最高價氧化物的水化物的堿性弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2、Br2、I2的熔點 | B. | Cl2、Br2、I2的相對分子質量 | ||
| C. | HCl、HBr、HI的酸性 | D. | 氫化物HCl、HBr、HI的熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有①③ | B. | 只有②③④ | C. | 只有①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 實驗內容 | 實驗目的 |
| A | 用石墨電極電解Mg(NO3)2、Pb( NO3)2 的混合液 | 比較確定鉛和鎂的金屬活動性強弱 |
| B | 測相同溫度下飽和Na2CO3溶液和飽和Na2SiO3溶液的pH | 確定碳和硅兩元素非金屬性強弱 |
| C | 室溫下,用pH計測定濃度為0.1mol•L-1NaClO溶液和0.1mol•L-1CH3COONa溶液的pH | 比較HClO和CH3COOH的酸性強弱 |
| D | 室溫下,分別向2支試管中加入相同體積、相同濃度的Na2S2O3溶液,再分別加入相同體積不同濃度的稀硫酸 | 研究濃度對反應速率的影響 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com