
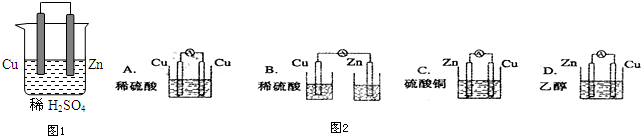
分析 (1)銅、鋅、稀硫酸原電池中,鋅易失電子發生氧化反應而作負極,銅作正極,正極上氫離子得電子發生還原反應;
(2)銅、鋅、稀硫酸原電池中,鋅易失電子溶解發生氧化反應,銅作正極,正極上氫離子得電子生成氫氣;
(3)根據原電池的構成條件分析,原電池的構成條件是:①有兩個活潑性不同的電極,②將電極插入電解質溶液中,③兩電極間構成閉合回路,④能自發的進行氧化還原反應.
解答 解:(1)銅、鋅、稀硫酸原電池中,鋅易失電子發生氧化反應而作負極,電極反應式為:Zn-2e-═Zn2+,銅作正極,正極上氫離子得電子發生還原反應,電極反應式為:2H++2e-=H2↑,總反應為Zn+2H+=Zn2++H2↑,
故答案為:負;Zn-2e-═Zn2+;正;2H++2e-=H2↑;Zn+2H+=Zn2++H2↑;
(2)銅作正極,正極上氫離子得電子發生還原反應,電極反應式為:2H++2e-=H2↑,所以銅極上可以觀察到有氣泡產生;鋅易失電子發生氧化反應而作負極,電極反應式為:Zn-2e-═Zn2+,所以鋅極可以觀察到鋅片逐漸溶解;
故答案為:有氣泡產生;鋅片逐漸溶解;
(3)A、兩個電極材料相同且不能自發的進行氧化還原反應,故A錯誤.
B、沒有形成閉合回路,故B錯誤.
C、符合原電池的構成條件,故C正確.
D、乙醇不是電解質溶液且不能自發的進行氧化還原反應,故D錯誤.
故選C.
點評 本題考查了原電池原理以及形成原電池的條件,明確正負極的判斷方法、正負極上電極反應即可解答,難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
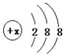 有幾種元素的微粒電子層結構如圖所示,其中:
有幾種元素的微粒電子層結構如圖所示,其中: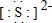 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| B12結構單元 | SF6分子 | S8分子 | HCN | |
| 結構模型示意圖 |  |  |  |  |
| 備注 | 熔點1873K | / | 易溶于CS2 | / |
| A. | 單質B結構單元中含有30個B-B鍵,含20個正三角形 | |
| B. | SF6是由極性鍵構成的非極性分子 | |
| C. | 固態硫S8中S原子為sp2雜化 | |
| D. | HCN的結構式為H-C≡N |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HBrO4的酸性比HClO4的酸性強 | |
| B. | 砹(At)為有色固體,AgAt難溶于水也不溶于稀硝酸 | |
| C. | 在氧氣中,銣(Rb)的燃燒產物比鈉的燃燒產物更復雜 | |
| D. | 硒化氫(H2Se)是無色、有毒且無硫化氫穩定的氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 最近有研究人員發現了一種處理高濃度乙醛廢水的新方法-隔膜電解法,乙醛分別在陰、陽極發生反應,轉化為乙醇和乙酸.實驗室以一定濃度的乙醛-Na2SO4溶液為電解質溶液,模擬乙醛廢水的處理過程,其裝置如圖所示.下列說法正確的是( )
最近有研究人員發現了一種處理高濃度乙醛廢水的新方法-隔膜電解法,乙醛分別在陰、陽極發生反應,轉化為乙醇和乙酸.實驗室以一定濃度的乙醛-Na2SO4溶液為電解質溶液,模擬乙醛廢水的處理過程,其裝置如圖所示.下列說法正確的是( )| A. | 若以CH4-空氣燃料電池為直流電源,燃料電池的b極應通入空氣 | |
| B. | 電解過程中,生成0.1 mol乙酸的同時,有0.2 mol的乙醇生成 | |
| C. | 陽極反應CH3CHO-2e-+OH-═CH3COOH+H+ | |
| D. | 電解過程中兩極除分別生成乙酸和乙醇外,均產生了無色氣體,則陽極產生的是O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A>B>D>C | B. | B>D>A>C | C. | D>B>A>C | D. | D>A>B>C |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
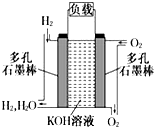 被譽為改變未來世界的十大新科技之一的燃料電池具有無污染、無噪音、高效率的特點.如圖為氫氧燃料電池的結構示意圖,電解質溶液為KOH溶液,電極材料為疏松多孔石墨棒.當氧氣和氫氣分別連續不斷地從正、負兩極通入燃料電池時,便可在閉合回路中不斷地產生電流.試回答下列問題:
被譽為改變未來世界的十大新科技之一的燃料電池具有無污染、無噪音、高效率的特點.如圖為氫氧燃料電池的結構示意圖,電解質溶液為KOH溶液,電極材料為疏松多孔石墨棒.當氧氣和氫氣分別連續不斷地從正、負兩極通入燃料電池時,便可在閉合回路中不斷地產生電流.試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
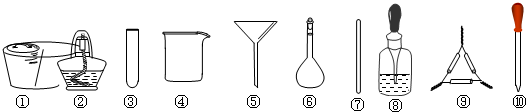
| A. | 將干海帶剪碎后灼燒灰化,選用①、②和⑨ | |
| B. | 將海帶灰加入蒸餾水攪拌煮沸,選用④、⑥和⑦ | |
| C. | 過濾得到的濾液,選用④、⑤和⑦ | |
| D. | 檢驗濾液中的I-,選用③、⑧和⑩ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:W>Z>Y>X | |
| B. | Y元素在周期表中的位置為第三周期第IVA族 | |
| C. | 與氫氣化合時,Z比Y容易 | |
| D. | 甲中只含有離子鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com