
| A. | CO2、SiO2的晶體結構類型不同 | |
| B. | 加熱硅、硫晶體使之熔化,克服的作用力不同 | |
| C. | HF比HCl穩(wěn)定是因為HF間存在氫鍵 | |
| D. | NaOH、NH4Cl晶體中既有離子鍵又有共價鍵 |
分析 A、二氧化碳是分子晶體;二氧化硅是原子晶體;
B、硅是原子晶體,而硫是分子晶體;
C、穩(wěn)定性是化學性質(zhì);
D、NaOH是含共價鍵的離子化合物、NH4Cl是含共價鍵的離子化合物.
解答 解:A、二氧化碳是分子晶體;二氧化硅是原子晶體,所以兩者的晶體結構類型不同,故A正確;
B、硅是原子晶體,而硫是分子晶體,兩晶體熔化,克服的作用力分別是共價鍵和分子間作用力,故B正確;
C、穩(wěn)定性是化學性質(zhì),因為非金屬性F強于Cl,所以HF比HCl穩(wěn)定,與氫鍵無關,故C錯誤;
D、NaOH是含共價鍵的離子化合物、NH4Cl是含共價鍵的離子化合物,所以NaOH、NH4Cl晶體中既有離子鍵又有共價鍵,故D正確;
故選C.
點評 本題考查了晶體類型的判斷等知識點,根據(jù)晶體的構成微粒確定晶體類型,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | NH4HCO3溶液與過量KOH濃溶液:NH4++OH-═NH3↑+H2O | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好為中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 稀硝酸和過量的鐵屑反應:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | Fe(OH)3溶于氫碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,100 mL 1 mol•L-1 Na2CO3溶液中含有的陰離子數(shù)大于0.1NA | |
| B. | 常溫常壓下,28g14CO和N2的混合物所含的質(zhì)子數(shù)為14NA | |
| C. | 將NA個NH3分子溶于1L水中得到1 mol•L-1的氨水 | |
| D. | 1molCl2分別與足量的鐵或氫氧化鈉溶液反應,轉移電子數(shù)均為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬可用作凈水劑 | |
| B. | 熱的純堿溶液可用于除去物品表面的油污 | |
| C. | 銨態(tài)氮肥和草木灰(主要成分碳酸鉀)不能混合使用 | |
| D. | 配制FeCl2溶液時需要向溶液中加少量鐵粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧氣是氧化產(chǎn)物 | |
| B. | O2F2是氧化劑 | |
| C. | 若生成 4.48 L HF,則轉移 0.8 mol 電子 | |
| D. | 還原劑與氧化劑的物質(zhì)的量之比為 4:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 次氯酸有酸性,可用于漂白、殺菌消毒 | |
| B. | 純堿能與酸反應,可用作治療胃酸過多的藥物 | |
| C. | 液氨汽化時要吸收大量的熱,工業(yè)上可用作制冷劑 | |
| D. | 晶體硅的熔點高、硬度大,可用于制作半導體材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
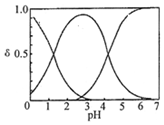 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三種形態(tài)的粒子的分布分數(shù)δ隨溶液pH變化的關系如圖所示[已知Ksp(CaC2O4)=2.3×10-9].下列說法正確的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三種形態(tài)的粒子的分布分數(shù)δ隨溶液pH變化的關系如圖所示[已知Ksp(CaC2O4)=2.3×10-9].下列說法正確的是( )| A. | 0.1mol•L-1H2C2O4溶液使KMnO4溶液褪色的離子方程式:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| B. | 0.1 mol•L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5時,溶液中主要含碳微粒濃度大小關系為:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 一定溫度下,往CaC2O4飽和溶液中加入少量CaCl2固體,c(C2O42-)將減小,c(Ca2+)不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 把鐵片與電源正極相連、碳棒與電源負極相連放入食鹽水中,證明鐵被保護 | |
| B. | 電解AlCl3溶液制取鋁單質(zhì) | |
| C. | 用25 mL滴定管量出14.80 mL溶液 | |
| D. | 用pH試紙測得某堿溶液的pH為12.6 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com