
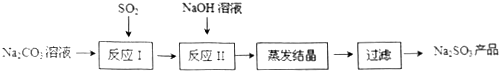
分析 碳酸鈉溶液中通入二氧化硫依次發生的反應為Ⅰ:2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3,2NaHCO3+SO2=Na2SO3+CO2,SO2+Na2SO3=2NaHSO3,反應Ⅱ是加入氫氧化鈉溶液發生反應:NaHSO3+NaOH=Na2SO3+H2O(主要),SO2+2NaOH=Na2SO3+H2O(次要),得到亞硫酸鈉溶液蒸發濃縮、冷卻結晶過濾洗滌得到Na2SO3.
(1)二氧化硫與水反應生成亞硫酸,又被氧化為硫酸;
(2)Na2CO3溶液呈堿性;
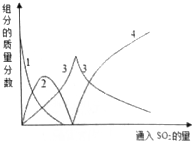
(3)依據反應過程和圖象曲線變化可知,圖象3表示的是亞硫酸鈉,圖象2表示的是碳酸氫鈉;
(4)“反應II”中加入NaOH溶液的目的是和亞硫酸氫鈉反應得到亞硫酸鈉;
(5)Na2SO3被空氣氧化成Na2SO4.
解答 解:(1)二氧化硫與水反應生成亞硫酸,又被氧化為硫酸,則SO2形成硫酸型酸雨,故答案為:酸雨;
(2)亞硫酸的酸性比碳酸強,故用Na2CO3溶液能吸收SO2,故答案為:亞硫酸的酸性比碳酸強;
(3)依據反應過程和圖象曲線變化可知,圖象3表示的是亞硫酸鈉,線2表示的組分為NaHCO3,故答案為:NaHCO3;
(4)“反應II”中加入NaOH溶液的目的是和亞硫酸氫鈉反應得到亞硫酸鈉,反應的化學方程式為:NaHSO3+NaOH=Na2SO3+H2O(主要)、SO2+2NaOH=Na2SO3+H2O(次要),
故答案為:NaHSO3+NaOH=Na2SO3+H2O(主要)、SO2+2NaOH=Na2SO3+H2O(次要);
(5)Na2SO3產品久置后質量變重,主要原因是Na2SO3被空氣中氧氣氧化成Na2SO4,
故答案為:Na2SO3被空氣中氧氣氧化成Na2SO4.
點評 本題考查了無機物制備流程、反應原理及其物質組成的實驗測定,題目難度中等.


科目:高中化學 來源:2017屆廣東省山一高三上第二次統測化學試卷(解析版) 題型:選擇題
下列各組物質中,物質之間通過一步反應就能實現圖示變化的是( )
物質編號 | 物質轉化關系 | a | b | c | d |
A |
| N2 | NO2 | NO | HNO3 |
B | Na | Na2O2 | NaOH | NaCl | |
C | Si | SiO2 | H2SiO3 | Na2SiO3 | |
D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
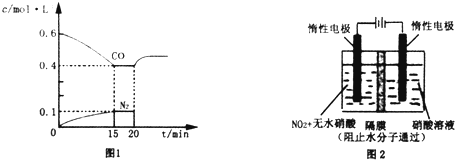
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
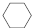 (g)$?_{高溫}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高溫}^{Pt-Sn/Al_{2}O_{3}}$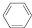 (g)+3H2(g).
(g)+3H2(g).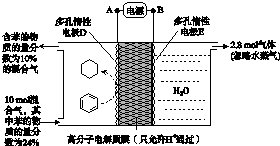
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
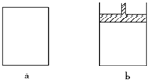 有a、b兩個極易導熱的密閉容器,a保持容積不變,b中的活塞可上下移動,以保持內外壓強相等.在相同條件下將3molA、1molB分別同時混合于a、b兩容器中,發生反應:
有a、b兩個極易導熱的密閉容器,a保持容積不變,b中的活塞可上下移動,以保持內外壓強相等.在相同條件下將3molA、1molB分別同時混合于a、b兩容器中,發生反應:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 混合物 | B. | 單質 | C. | 氧化物 | D. | 化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 (1)為了檢驗和除去表中的各種雜質(括號里的為雜質),請從①中選出適當的檢驗試劑,從②中選出適當的除雜試劑,將所選的答案用字母填入相應的空格內.
(1)為了檢驗和除去表中的各種雜質(括號里的為雜質),請從①中選出適當的檢驗試劑,從②中選出適當的除雜試劑,將所選的答案用字母填入相應的空格內.| 物質 | 檢驗試劑 | 除雜試劑 |
| 甲烷(乙烯) | ||
| 酒精(水) |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
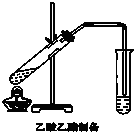
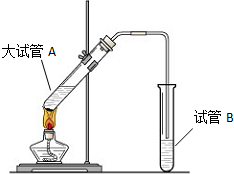 “酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如圖所示的裝置制取乙酸乙酯.回答下列問題:
“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如圖所示的裝置制取乙酸乙酯.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com