
| A. | 任何化學反應都伴隨著能量的變化 | |
| B. | 升高溫度或加入催化劑,可以改變化學反應的反應熱 | |
| C. | 化學反應中的能量變化都是以熱量的形式體現 | |
| D. | 2CO(g)+O2(g)═2CO2(g)△H<0,則56g CO和32g O2所具有的總能量小于88g CO2所具有的總能量 |
分析 A.化學反應的實質是舊化學鍵的斷裂和新化學鍵的形成;
B.使用催化劑只能改變反應速率,反應熱和反應物以及生成物的能量有關;
C.能量變化可以是熱能、電能、光能等;
D.放熱反應中反應物的總能量大于生成物的總能量.
解答 解:A.化學反應的實質是舊化學鍵的斷裂和新化學鍵的形成,舊鍵斷裂吸收能量,新鍵形成要放出能量,所以任何化學反應都伴隨著能量的變化,故A正確;
B.使用催化劑前后,反應物和生成物的能量是不變化的,化學反應的反應熱是不變的,故B錯誤;
C.化學反應中一定伴隨能量變化,能量變化可以是熱能、電能、光能等,故C錯誤;
D.2CO(g)+O2(g)═2CO2(g)△H<0,該反應為放熱反應,反應物的總能量大于生成物的總能量,則56g CO和32g O2所具有的總能量大于88g CO2,故D錯誤.
故選A.
點評 本題考查了化學反應的能量變化,題目涉及化學鍵與能量的關系、催化劑對反應的影響、能量轉化形式等,題目難度不大,把握能量守恒和斷裂化學鍵吸收能量,形成化學鍵放出能量是解題關鍵.


 小學課時特訓系列答案
小學課時特訓系列答案科目:高中化學 來源: 題型:實驗題
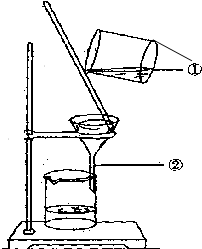 如圖為某學生進行粗鹽提純實驗中過濾操作的示意圖,試回答:
如圖為某學生進行粗鹽提純實驗中過濾操作的示意圖,試回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高溫度能加快反應速率的主要原因,是增加了反應物分子中活化分子的百分數 | |
| B. | 正反應是吸熱反應,達到平衡時,升高溫度,v正增大,v逆減小,所以平衡向正反應方向移動 | |
| C. | 一定條件下增大反應物的量,一定會加快反應速率 | |
| D. | 對于任何一個化學反應,用其中任何一種反應物濃度的減小來表示化學反應速率,都是相同的數值 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 準確稱取0.4000 g NaOH固體可配成100 mL 0.1000 mol•L-1的NaOH標準溶液 | |
| B. | 催化劑可以加快化學反應速率但不能改變化學反應的焓變 | |
| C. | 100 mL pH=3的HA和HB分別與足量的鋅反應,HB放出的氫氣多,說明HB酸性比HA弱 | |
| D. | 對于反應2SO2(g)+O2(g)?2SO3(g),壓縮氣體體積使壓強增大(其他條件不變),則SO2的轉化率增大,平衡常數K也增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
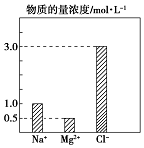 某100mL溶液中含有的部分離子濃度大小如圖所示,該溶液可能還含有Fe3+、Ba2+、H+、SO42-、CO32-.為了進一步確認,對該溶液進行實驗檢測:
某100mL溶液中含有的部分離子濃度大小如圖所示,該溶液可能還含有Fe3+、Ba2+、H+、SO42-、CO32-.為了進一步確認,對該溶液進行實驗檢測:| 實驗操作與現象 | 實驗結論 | 判斷理由 | |
| 步驟一 | 仔細觀察坐標圖 | 肯定無 CO32- | 肯定無該離子的理由碳酸根離子和鎂離子之間會反應 |
| 步驟二 | 該溶液呈無色、透明、均一狀態 | 肯定無 Fe3+ | 肯定無該離子的理由該離子為黃色 |
| 步驟三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42-、H+;肯定無Ba2+ | 肯定有H+的理由電荷守恒 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某課外小組利用下列裝置,對濃硫酸與乙醇反應的可能產物進行了如下探究.
某課外小組利用下列裝置,對濃硫酸與乙醇反應的可能產物進行了如下探究.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com