
| A. | $\frac{a}{4b}$mol-1 | B. | $\frac{b}{4a}$mol-1 | C. | $\frac{a}{4b}$ | D. | $\frac{b}{4a}$ |
 全優沖刺100分系列答案
全優沖刺100分系列答案 英才點津系列答案
英才點津系列答案 紅果子三級測試卷系列答案
紅果子三級測試卷系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ,H2O2的結構式為H-O-O-H,N-H鍵的鍵能為a kJ•mol-1,N-N鍵的鍵能為b kJ•mol-1,H-O鍵的鍵能為c kJ•mol-1,O-O鍵的鍵能為d kJ•mol-1,
,H2O2的結構式為H-O-O-H,N-H鍵的鍵能為a kJ•mol-1,N-N鍵的鍵能為b kJ•mol-1,H-O鍵的鍵能為c kJ•mol-1,O-O鍵的鍵能為d kJ•mol-1, 鍵的鍵能為e kJ•mol-1,則1mol N2H4與足量H2O2反應的熱化學方程式為N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=(4a+b-4c+d-e)kJ•mol-1.
鍵的鍵能為e kJ•mol-1,則1mol N2H4與足量H2O2反應的熱化學方程式為N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=(4a+b-4c+d-e)kJ•mol-1.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 1mol Ne含有的電子數目為10NA | |
| B. | 0.2NA個硫酸分子與19.6g磷酸含有相同的氧原子數 | |
| C. | 2.8g氮氣所含的分子數為NA | |
| D. | 1.8gNH4+中含有的質子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
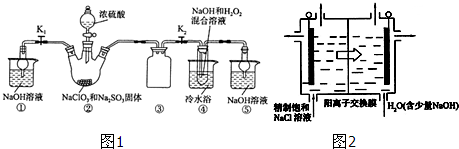
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 CO32-+7H2O.
CO32-+7H2O.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com