
| 實驗步驟 | 預期現象和結論 |
| 步驟1:用試管取樣品溶液2~3mL,再用滴管取LKSCN溶液,向試管中滴入1~2滴0.1mol/LKSCN溶液 | (1)若出現紅色,則假設1成立; (2)若未出現紅色,則假設2或假設3成立. |
步驟2:另取2~3mL樣品溶液于試管中滴入1~2mL品紅稀溶液 | 1若品紅溶液紅色褪色,假設2成立; 2若品紅溶液不褪色,結合步驟1中的(2)則假設3成立 |
分析 (1)二氧化硫可以被三價鐵氧化為硫酸根離子,三價鐵自身被還原為亞鐵離子,結合原子守恒分析,化合價升高元素所在的產物是氧化產物;
(2)硫酸根可以和鋇離子反應生成白色沉淀,但是要排除碳酸根的干擾;
(3)三價鐵離子具有氧化性,亞硫酸具有還原性,二者不能組合,三價鐵能使硫氰酸鉀顯紅色,二氧化硫能使品紅褪色,據此來分析存在的微粒.
解答 解:(1)二氧化硫可以被三價鐵氧化為硫酸根離子,三價鐵自身被還原為亞鐵離子,所以產物有氯化亞鐵和硫酸以及鹽酸,反應的離子方程式為SO2+2H20+2Fe3+=2Fe2++SO42-+4H+,
故答案為:SO2+2H20+2Fe3+=2Fe2++SO42-+4H+;
(2)Fe3+能夠把H2SO3氧化成SO42-,溶液中存在硫酸根離子,證明反應發生了,硫酸根可以和鋇離子反應生成白色沉淀,但是要排除碳酸根的干擾,所以硫酸根的檢驗方法是:取少量樣品溶液于試管中,先滴入足量的稀鹽酸,再滴入氯化鋇溶液,有白色沉淀生成,
故答案為:取少量樣品溶液于試管中,先滴入足量的稀鹽酸,再滴入氯化鋇溶液,有白色沉淀生成;
(3)①三價鐵離子具有氧化性,亞硫酸具有還原性,二者不能組合,所以假設2:溶液中存在Fe2+、H2SO3,故答案為:Fe2+、H2SO3;
②三價鐵能使硫氰酸鉀顯紅色,亞硫酸中的二氧化硫能使品紅褪色,檢驗三價鐵可以將0.1mol/LKSCN溶液1~2滴加到待測樣品中,檢驗亞硫酸可以將品紅滴到樣品中,驗證時不能使用KMnO4溶液,因它可以同時氧化Fe2+和H2SO3,由于用FeCl3溶液吸收制取SO2氣體,Fe3+可以氧化H2SO3,故Fe3+與H2SO3不能共存,溶液中有H2SO3就一定有Fe2+.所以用品紅驗證了H2SO3的存在就不必再驗證Fe2+,
故答案為:
| 實驗步驟 | 預期現象和結論 |
| 步聚1:向試管中滴入1~2滴0.1mol/LKSCN溶液 | |
| 步驟2:另取2~3mL樣品溶液于試管中滴入1~2mL品紅稀溶液 | 1若品紅溶液紅色褪色,假設2成立; 2若品紅溶液不褪色,結合步驟1中的(2)則假設3成立 |
點評 本題考查物質組成與性質的實驗探究,為高頻考點,把握物質的性質、氧化還原反應原理、離子檢驗等為解答的關鍵,側重分析與實驗能力的考查,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
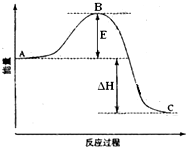 2SO2(g)+O2(g)═2SO3(g)反應過程的能量變化如圖所示.已知1mol SO2(g)氧化為1mol SO3(g)的△H=-99kJ•mol-1.請回答下列問題:
2SO2(g)+O2(g)═2SO3(g)反應過程的能量變化如圖所示.已知1mol SO2(g)氧化為1mol SO3(g)的△H=-99kJ•mol-1.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
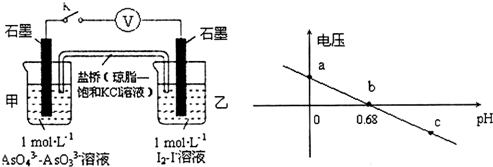
| A. | a點時,鹽橋中K+向左移動 | |
| B. | b點時,反應處于化學平衡狀態 | |
| C. | c點時,正極的電極反應為AsO43-+2H++2e-=AsO33-+H2O | |
| D. | pH>0.68時,氧化性I2>AsO43- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 混合氣體中NO與O2的體積之比為4:1 | |
| B. | 水吸收后的剩余氣體是O2,且c=$\frac{a}{6}$ | |
| C. | 取m g AgNO3溶于水再加足量鹽酸可生成沉淀$\frac{2a}{3×22.4}$×143.5g | |
| D. | 水吸收后所得溶液中HNO3的物質的量濃度為$\frac{b}{108}$mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
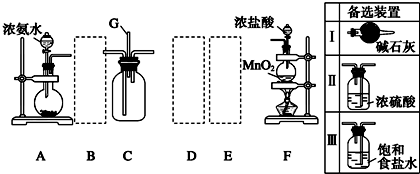
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| a | b | c | |
| A | 2 | 1 | 1 |
| B | 1 | 1 | 0 |
| C | 1 | 0 | 1 |
| D | 0 | 1 | 2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4種 | B. | 6種 | C. | 7種 | D. | 8種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 時間/h | 0 | 1 | ||
| pH | 4.7 | 4.6 | 4.56 | 4.55 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com