
【題目】某研究性學習小組請你參與“研究鐵與水反應所得固體物質的成分、性質及再利用”實驗探究,并共同解答下列問題:
探究一 設計如圖所示裝置進行“鐵與水反應”的實驗(夾持儀器略)。
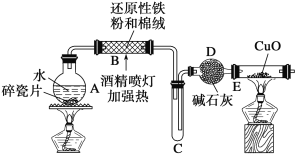
(1)硬質玻璃管B中發生反應的化學方程式為__________________________。
(2)反應前A中投放碎瓷片的目的是____________________。
(3)裝置E中的現象是________________________________。
探究二 設計如下實驗方案確定反應后硬質玻璃管B中黑色固體的成分。
(4)待硬質玻璃管B冷卻后,取少許其中的固體物質溶于稀硫酸后,將所得溶液分成兩份。
①一份滴加幾滴KSCN溶液。若溶液變血紅色,推斷硬質玻璃管B中固體物質的成分為________(選填序號,下同);若溶液未變血紅色,推斷硬質玻璃管B中固體物質的成分為________。
A.一定有Fe3O4 B.一定有Fe C.只有Fe3O4 D.只有Fe
② 另一份用膠頭滴管滴加酸性KMnO4溶液,若溶液褪色,可以證明溶液中存在 (填離子符號)。
③ 下列試劑中,不能使Fe3+轉化為Fe2+的是
A.氯氣
B.Fe
C.H2O2
D.稀硝酸
E.Cu
【答案】(1)3Fe+4H2O(g)![]() Fe3O4+4H2 (2)(1分)防止暴沸
Fe3O4+4H2 (2)(1分)防止暴沸
(3)(1分)黑色固體變紅,右端管壁有水珠
(4)①A ; B ② Fe2+ ③ A C D(全對2分,漏選1分,錯選0分)
【解析】
試題分析:【探究一】(1)硬質管中鐵與水蒸氣在高溫下反應生成四氧化三鐵和氫氣,反應的化學方程式為:3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)液體加熱時容易發生暴沸現象,加入碎瓷片的作用是防止暴沸;
(3)裝置E中發生反應為:H2+CuO![]() Cu+H2O,則反應現象是:黑色固體變紅,右端管壁有水珠;
Cu+H2O,則反應現象是:黑色固體變紅,右端管壁有水珠;
【探究二】(4)在驗證反應后黑色固體的成分時,檢驗Fe3+,最佳試劑為KSCN溶液;在確定存在Fe3+時,檢驗Fe2+,可用酸性KMnO4溶液.由于酸性KMnO4溶液與鹽酸發生反應,所以在溶解反應后的黑色固體時,不能用鹽酸,也不能用硝酸(因為HNO3可氧化Fe2+),可用稀硫酸;
①一份滴加幾滴KSCN溶液,若溶液變血紅色,說明溶液中含有鐵離子,則可推斷硬質玻璃管B中固體物質的成分為:A.一定有Fe3O4;若溶液未變血紅色,則溶液中不存在鐵離子,可推斷硬質玻璃管B中固體物質中一定存在Fe,即B正確,故答案為AB;
②用膠頭滴管加入酸性高錳酸鉀溶液,若酸性高錳酸鉀溶液褪色,則證明溶液中含有亞鐵離子;
③Fe3+轉化為Fe2+的過程是還原過程,需要添加還原劑,而氯氣、H2O2、稀硝酸均具有強氧化性,只能將Fe2+氧化為Fe3+,故答案為ACD。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】2015年8月12日晚11時,天津港國際物流中心區域內化學危險品倉庫因起火而發生爆炸。其倉庫存儲的桶裝氰化鈉,因爆炸沖擊發生了泄漏。氰化鈉是一種重要的基本化工原料,用于電鍍、冶金等,因此很多工業廢水中也含氰化鈉,此工業廢水可與其他工業廢水一同處理。下圖是工業上處理含鉻廢水和含氰廢水的流程圖:
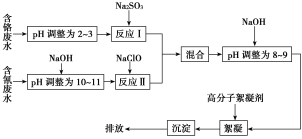
(1)含鉻廢水中的鉻元素主要以CrO![]() 形式存在,酸化時CrO
形式存在,酸化時CrO![]() 可轉化為Cr2O
可轉化為Cr2O![]() ,現象是__________________________。
,現象是__________________________。
(2)酸性條件下,Cr2O![]() 極易被還原劑還原為毒性較小的Cr3+。圖中“反應Ⅰ”的離子方程式為__________________________。
極易被還原劑還原為毒性較小的Cr3+。圖中“反應Ⅰ”的離子方程式為__________________________。
(3)①在爆炸發生時有少量氰化鈉炸出,有人指出可用雙氧水處理,使之被氧化成無毒物質,已知二者反應生成一種烘焙時常用的物質,并釋放出一種有刺激性氣味的氣體,該氣體易液化,液化后常用作制冷劑,請寫出氰化鈉與過氧化氫反應的化學方程式:________________________。
②除雙氧水外,還可用硫代硫酸鈉處理氰化鈉,轉化為Na2SO3及弱毒性的NaSCN,寫出兩種物質發生反應的化學方程式:__________________。
(4)pH>10時,“反應Ⅱ”中的NaClO可將氰離子(CN-)快速氧化為兩種無毒的物質,寫出該反應的離子方程式:_____________________________。
(5)經過“反應Ⅰ”和“反應Ⅱ”的兩種廢水“混合”的目的是____________________。
向混合后的溶液中加NaOH調為堿性的目的是______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將5molL﹣1的鹽酸10mL稀釋到200mL,再取出5mL,這5mL溶液的物質的量濃度是( )
A.0.05 molL﹣1
B.0.25 molL﹣1
C.0.10 molL﹣1
D.0.50 molL﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)如圖所示,將氯氣依次通過盛有干燥有色布條的廣口瓶和盛有潮濕有色布條的廣口瓶,可觀察到的現象是 。
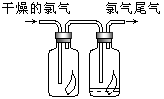
(2)為防止氯氣尾氣污染空氣,根據氯水顯酸性的性質,可用 溶液吸收多余的氯氣,原理是(用化學方程式表示)______________________________。
(3)根據這一原理,工業上常用廉價的石灰乳吸收工業氯氣尾氣制得漂白粉,漂白粉的有效成分是__________(填化學式),長期露置于空氣中的漂白粉,加稀鹽酸后產生的氣體是__________(用字母代號填)。
A.O2 B.H2 C.CO2 D.HClO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知1 g氫氣完全燃燒生成水蒸氣時放出熱量121 kJ,且氧氣中1 mol O=O鍵完全斷 裂時吸收熱量496 kJ,氫氣中1 mol H―H鍵斷裂時吸收熱量為436 kJ,求水蒸氣中1 mol H―O鍵形成時放出熱量( )
A. 463kJ B. 557 kJ C. 486kJ D.188 kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成兩份,向其中一份中逐漸加入銅粉,最多能溶解19.2 g(已知硝酸只能被還原為NO氣體)。向另一份中逐漸加入鐵粉,產生氣體的量隨鐵粉質量增加的變化如圖所示。下列分析或結果錯誤的是( )
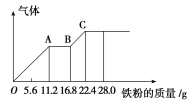
A.混合酸液中NO![]() 的物質的量為0.4 mol
的物質的量為0.4 mol
B.OA段產生是NO,AB段反應為2Fe3++Fe=3Fe2+,BC段產生氫氣
C.溶液中最終溶質為FeSO4
D.c(H2SO4)為5 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將下圖所示實驗裝置的 K 閉合,下列判斷正確的是
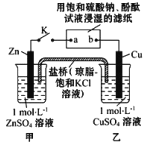
A.片刻后甲池中 c(SO42-)增大 B.電子沿 Zn→a→b→Cu 路徑流動
C.Cu 電極上發生還原反應 D.片刻后可觀察到濾紙 b 點變紅色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com