

 2SO3(g)。反應體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:
2SO3(g)。反應體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:
 0(填“>’或“<”)。
0(填“>’或“<”)。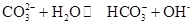 ,25℃時該反應的K=2×10-4mol·L-1,則當溶液中c(HCO- 3):c(CO2- 3)=2∶1時,溶液的pH= 。
,25℃時該反應的K=2×10-4mol·L-1,則當溶液中c(HCO- 3):c(CO2- 3)=2∶1時,溶液的pH= 。

 口算題天天練系列答案
口算題天天練系列答案科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.反應CO2(g)+C(s)=2CO(g)在高溫下可自發進行,則該反應的△H> 0 |
| B.工業上電解飽和食鹽水時,以石墨作陰極,鐵棒作陽極 |
| C.常溫下,0.1mol·L-1 CH3COOH溶液pH=1 |
| D.常溫下,在AgCl懸濁液中加入少量NaCl飽和溶液,c(Ag+)減小,Ksp(AgCl) 減小 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題




| A.向一定質量的鋅與過量的稀硫酸反應的試管中加入少量的CuSO4溶液,圖1虛線表示加入CuSO4溶液時氫氣體積與時間的關系 |
| B.用0.0100mol/L硝酸銀標準溶液,滴定濃度均為0.1000mol/LCl-、Br-及I-的混合溶液,由圖2曲線,可確定首先沉淀的是Cl- |
| C.向NH4Al(SO4)2溶液中滴加過量的NaOH溶液,圖3中曲線表示NaOH的物質的量與Al(OH)3物質的量關系圖 |
| D.由圖4可說明乙烯與H2加成反應是放熱反應,虛線表示在有催化劑條件下的反應進程 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
 CO(g) + 3H2(g) ΔH =" +206.2" kJ/mol
CO(g) + 3H2(g) ΔH =" +206.2" kJ/mol CO2(g) +4H2(g) ΔH = +165.0kJ/mol
CO2(g) +4H2(g) ΔH = +165.0kJ/mol

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.反應NH3(g)+HCl(g)=NH4Cl(s)低溫下能自發進行,說明該反應的△H<0 |
| B.Mg在空氣中燃燒時發出耀眼的白光,可用于制造信號彈 |
| C.純堿溶于熱水中去污效果增強,說明純堿的水解是吸熱反應 |
| D.反應N2(g)+3H2(g)=2NH3(g)(△H<0)達平衡后,降低溫度,正反應速率增大、逆反應速率減小,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題



| A.降低溫度 | B.增加了生成物 | C.減小壓強 | D.使用了高效催化劑 |


查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.凡是放熱反應都是自發的 |
| B.難溶電解質的溶解平衡是一種動態平衡 |
| C.利用沉淀反應除雜時,可使雜質離子完全沉淀 |
| D.pH=5的鹽酸稀釋1000倍后,溶液的pH增到8 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題


| A.向容器中按原比例再充入原料氣 | B.向容器中再充入惰性氣體 |
| C.改變反應的催化劑 | D.液化生成物分離出氨 |

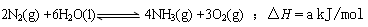
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |


查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com