
分析 (1)所含元素化合價降低的反應物為氧化劑,所含元素化合價升降的反應物為還原劑,據此結合元素化合價判斷;
(2)一氧化氮和一氧化碳經過排氣管中的催化轉化器轉化為對大氣無污染的物質,應生成氮氣、二氧化碳;
(3)尾氣中二氧化氮含量為1×106×0.5%=0.5×104L,結合反應的化學方程式計算.
解答 解:(1)產物NaNO2中N元素的化合價為+3,在反應①中,氧化劑是NO2,還原劑是NO,所以氧化劑與還原劑的質量之比為46:30=23:15,在反應②中,只有N元素化合價發生變化,N元素化合價分別由+4價升高到+5價、降低到+3價,NO2既是氧化劑又是還原劑,故答案為:+3,23:15,二氧化氮,二氧化氮;
(2)一氧化氮和一氧化碳經過排氣管中的催化轉化器轉化為對大氣無污染的物質,應生成氮氣、二氧化碳,反應方程式為:2NO+2CO$\frac{\underline{\;催化劑\;}}{\;}$N2+2CO2,
故答案為:2NO+2CO$\frac{\underline{\;催化劑\;}}{\;}$N2+2CO2;
(3)尾氣中二氧化氮含量為1×106L×0.5%=0.5×104L,設需要氨氣xmol
6NO2 +8NH3 ═7N2 +12H2O
6×22.4L 8mol
0.5×104 L x
解得:x=297.62mol.則氨氣的質量為297.62×17×10-3kg=5.06 kg,
故答案為:5.06.
點評 本題考查氧化還原反應,側重于學生的分析能力和計算能力的考查,為高頻考點,注意從元素化合價的角度認識相關概念,結合反應的化學方程式計算,難度中等.


科目:高中化學 來源: 題型:解答題
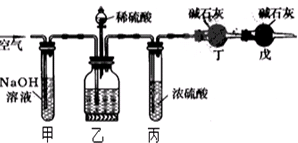
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,16gCH4含有10NA個電子 | |
| B. | 0.1mol•L-1的鹽酸溶液中含有0.1NA個H+ | |
| C. | 1molNa與乙醇完全反應,失去2NA個電子 | |
| D. | 標準狀況下,22.4L苯含有NA個苯分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
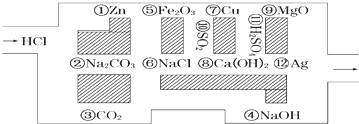
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
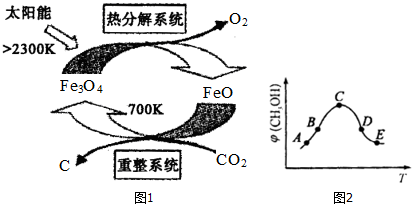
| 容器 | 甲 | 乙 |
| 反應物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、c molCH3OH(g)、c molH2O(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
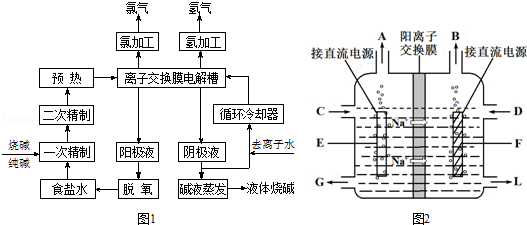
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液呈淺綠色 | |
| B. | 該溶液中加入NaOH溶液,生成白色沉淀并迅速變成灰綠色,最后變為紅褐色 | |
| C. | 向該溶液中加入氯水,再滴入幾滴KSCN溶液,呈紅色 | |
| D. | 向該溶液中滴入幾滴KSCN溶液,不變色,再加入氯水,呈紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
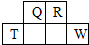 短周期元素Q、R、T、W在元素周期表中的位置如圖所示,其中T的單質既可與鹽酸反應,又可與NaOH溶液反應,請回答下列問題:
短周期元素Q、R、T、W在元素周期表中的位置如圖所示,其中T的單質既可與鹽酸反應,又可與NaOH溶液反應,請回答下列問題: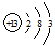 .
.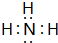
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com