
【題目】某研究性學習小組利用下圖裝置探究草酸亞鐵晶體(FeC2O4·2H2O)的分解產物,下列說法錯誤的是
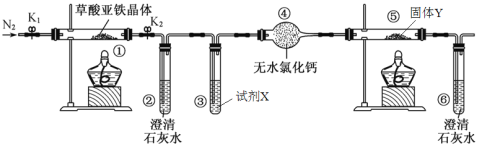
A. 實驗前通入N2的作用是排出裝置內的空氣
B. ②、⑥中澄清石灰水的作用均是為了檢驗CO2氣體
C. 裝置中試劑X為NaOH溶液,固體Y為CuO固體
D. 將①中所得固體溶于KSCN溶液,可以檢驗其中鐵元素的化合價
【答案】D
【解析】
A.反應裝置中含有空氣,若不將裝置中的空氣排出,會將草酸亞鐵分解產生的FeO氧化為Fe2O3,影響實驗測定,因此該操作合理,A正確;
B.②中澄清石灰水的作用是為了檢驗FeC2O4·2H2O 分解產物中含CO2氣體;⑥中澄清石灰水的作用是為了檢驗CO2氣體,進而證明FeC2O4·2H2O分解產生的物質中含CO,CO與⑤處的灼熱的CuO發生了反應產生了CO2,B正確;
C. FeC2O4·2H2O受熱分解產生的CO2氣體通過②檢驗出來,通過裝置中試劑X為NaOH溶液來除去,經無水氯化鈣干燥后經灼熱的固體Y反應轉化為CO2氣體,所以Y為CuO固體,C正確;
D.將①中所得固體為FeO,該物質在KSCN溶液中不能溶解,且其中含有的鐵元素為+2價,與KSCN也不能發生反應,因此不可以檢驗其中鐵元素的化合價,D錯誤;
故合理選項是C。


 浙江名校名師金卷系列答案
浙江名校名師金卷系列答案 全優沖刺100分系列答案
全優沖刺100分系列答案科目:高中化學 來源: 題型:
【題目】某原子的最外層電子排布為![]() ,下列對其核外電子運動的說法錯誤的是( )
,下列對其核外電子運動的說法錯誤的是( )
A. 有5種不同的運動范圍B. 有5種不同能量的電子
C. 有4種不同的伸展方向D. 有14種不同運動狀態的電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O2CrO42-(黃色)+2H+。用K2Cr2O7溶液進行下列實驗:
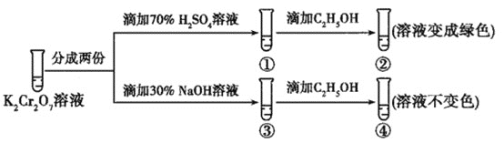
結合實驗,下列說法不正確的是( )
A.①中溶液橙色加深,③中溶液變黃
B.②中Cr2O72-被C2H5OH還原
C.對比②和④可知K2Cr2O7酸性溶液氧化性強
D.若向④中加入70%H2SO4溶液至過量,溶液變為橙色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列圖示與對應的敘述相符的是( )
A.圖1表示某恒溫密閉容器中反應CaCO3(s)![]() CaO(s)+CO2(g)達到平衡后,t1時刻壓縮容器體積,CO2的物質的量濃度隨時間的變化
CaO(s)+CO2(g)達到平衡后,t1時刻壓縮容器體積,CO2的物質的量濃度隨時間的變化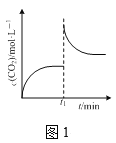
B.圖2表示Ksp=1.0×10-12的CdCO3飽和溶液中,c(Cd2+)與c(CO32-)的關系曲線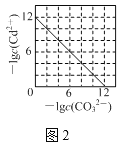
C.圖3表示其他條件一定時,反應2SO2(g)+O2(g)![]() 2SO3(g)在有、無催化劑條件下SO3的物質的量隨時間的變化曲線
2SO3(g)在有、無催化劑條件下SO3的物質的量隨時間的變化曲線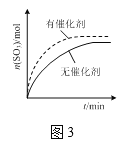
D.圖4表示燃燒熱為285.8kJ·mol-1的H2燃燒時能量的變化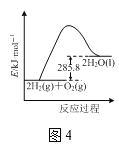
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C三個燒杯中分別盛有相同物質的量濃度的稀硫酸。
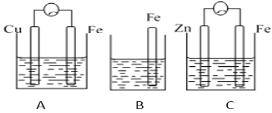
(1) B中反應的離子方程式為______。
(2) A中作正極的金屬是_____,該電極上看到的現象為_____。
(3) C中作負極的金屬是____,該電極反應方程式為______。
(4)現有未知金屬A,將A與Fe用導線相連后放入稀硫酸溶液中,觀察到A上有氣泡,在A上發生____反應。(填“氧化”或“還原”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,將NO2和O2的混合氣體12 mL通入足量水中,充分反應后剩余2 mL氣體(同溫同壓下),則原混合氣體中氧氣的體積為( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以工業級氧化鋅(含Fe2+、Mn2+、Cu2+、Ni2+等)為原料制備氧化鋅的流程如下:
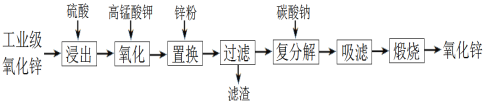
其中“氧化”加入KMnO4是為了除去浸出液中的Fe2+和Mn2+。下列有關說法錯誤的是
A. 浸出時通過粉碎氧化鋅提高了浸出率
B. “氧化”生成的固體是MnO2和Fe(OH)3
C. “置換”加入鋅粉是為了除去溶液中的Cu2+、Ni2+等
D. “煅燒”操作用到的儀器:玻璃棒、蒸發皿、泥三角
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是元素周期表的一部分,根據① ~ ⑨在周期表中的位置按題目要求回答:
族 周期 | IA | 0 | ||||||||
1 | ⅡA | …… …… …… | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
2 | ① | ② | ||||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||||
4 | ⑧ | ⑨ | ⑩ | |||||||
(1)畫出⑩的原子結構示意圖_________________________
(2)①與②形成的一種化合物甲,甲在大氣含量過高會產生溫室效應,寫出甲物質的結構式 __________________________________。
(3)元素③⑤對應的最高價氧化物的水化物,寫出它們相互之間能發生反應化學方程式__________________。
(4)元素⑦和⑨形成的化合物乙,請用電子式表示物質乙的形成過程__________________。
(5)②、⑥分別形成的兩種氫化物中,沸點較高的是______(填化學式),原因是:___________________________________________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2L密閉容器中充有2molSO2和一定量的O2,發生反應2SO2(g)+O2(g)![]() 2SO3(g)。當反應進行到4min時,測得此時SO2為0.4mol,則2min時密閉容器中SO3的物質的量為( )
2SO3(g)。當反應進行到4min時,測得此時SO2為0.4mol,則2min時密閉容器中SO3的物質的量為( )
A.1.6molB.1.2molC.大于1.6molD.小于1.2mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com