
 ZnO+2MnO(OH).下列說法正確的是( )
ZnO+2MnO(OH).下列說法正確的是( )

科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
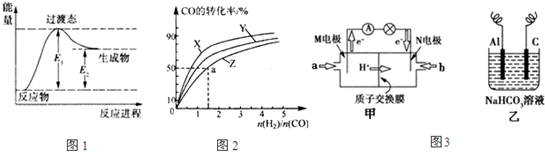
| ||
查看答案和解析>>
科目:高中化學 來源:2012-2013學年廣東省四校聯考化學試卷(解析版) 題型:推斷題
X、Y、Z、U、V是元素周期表前四周期中的五種常見元素,其相關信息如下表:
|
元素 |
相關信息 |
|
X |
地殼中含量最多的金屬,其氧化物可用作耐火材料 |
|
Y |
單質在常溫常壓下為黃綠色氣體 |
|
Z |
常溫常壓下,單質是淡黃色固體,常在火山口附近沉積 |
|
U |
常溫下單質遇濃硫酸鈍化,其一種核素的質量數為56,中子數為30 |
|
V |
屬短周期元素,原子的最外層電子數是內層電子數的2/5 |
請回答下列問題:
(1)元素X位于周期表中第 周期第 族,其離子結構示意圖為 。
(2)上述元素中最高價氧化物對應的水化物酸性最強的是 (寫化學式),非金屬氣態氫化物還原性最強的是 (寫化學式)。
(3)在堿性條件下,Y的單質可與UO2-反應制備一種可用于凈水的鹽UO42-,該反應的離子方程式是 。
(4)我國首創的海洋電池被大規模用于海洋燈塔。該電池是以X板為負極,鉑網為正極,海水為電解質溶液,電池總反應為:4X+3O2+6H2O=4X(OH)3。該電池正極反應為 。
(5)已知25℃時,Ksp[U(OH)3]=2.63×10-39,則該溫度下反應U(OH)3+3H+ U3++3H2O的平衡常數K=
。
U3++3H2O的平衡常數K=
。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年寧夏高三第二次模擬考試(理綜)化學部分 題型:填空題
“低碳循環”引起各國的高度重視,而如何降低大氣中CO2的含量及有效地開發利用CO2,引起了全世界的普遍重視。所以“低碳經濟”正成為科學家研究的主要課題
(1)用電弧法合成的儲氫納米碳管常伴有大量的碳納米顆粒(雜質),這種顆粒可用如下氧化法提純,請完成該反應的化學方程式:(系數按順序填在答題卷上)
___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
(2)將不同量的CO(g)和H2O(g)分別通入到體積為2L的恒容密閉容器中,進行反應CO(g)+H2O(g) CO2(g)+H2(g),得到如下三組數據:
CO2(g)+H2(g),得到如下三組數據:
|
實驗組[來源:] |
溫度℃ |
起始量/mol源:Z。xx。k.Com] |
平衡量/mol |
達到平衡所需時間/min[來源:學*科*網Z*X*X*K] |
||
|
CO |
H2O |
H2 |
CO |
|||
|
1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
|
2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
①實驗1中以v (CO2) 表示的反應速率為 (取小數二位,下同)。
②該反應為 (填“吸”或“放”)熱反應,實驗2條件下平衡常數K= 。
(3)已知在常溫常壓下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式:
⑷某實驗小組依據甲醇燃燒的反應原理,設計如右圖所示的電池裝置。

①該電池正極的電極反應為 。
② 工作一段時間后,測得溶液的pH減小,該電池總反應的化學方程式為 。
(5)CO2在自然界循環時可與CaCO3反應,CaCO3是一種難溶物質,其Ksp=2.8×10—9。CaCl2溶液與Na2CO3溶液混合可形成CaCO3沉淀,現將等體積的CaCl2溶液與Na2CO3溶液混合,若Na2CO3溶液的濃度為2×10—4mo1/L ,則生成沉淀所需CaCl2溶液的最小濃度為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
I.光伏組件采用高效率單晶硅或多晶硅光伏電池、高透光率鋼化玻璃、抗腐蝕鋁合多邊框等材料,使用先進的真空層壓工藝及脈沖焊接工藝制造。
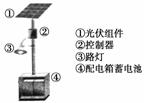 (1)下圖是太陽能電池板經太陽光照射前后內部電子的變化情況,圖乙中燈泡變亮,其中____(填寫“N”或“P”)是正極。
(1)下圖是太陽能電池板經太陽光照射前后內部電子的變化情況,圖乙中燈泡變亮,其中____(填寫“N”或“P”)是正極。
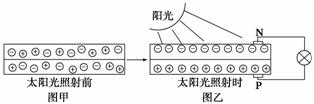
![]() (2)右上圖是一個太陽能路燈,圖中的④是蓄電池。鎳氫電池就是這樣一種與太陽能電池配套使用的蓄電池,白天用于充電,夜間供電。這種蓄電池容量大,充電放電循環壽命也較長。該蓄電池的總反應為Ni(OH)2 NiOOH+1/2H2↑。鎳氫電池的電解液采用30%的KOH溶液,白天充電反應時的陽極反應式為 ,夜間放電時,負極附近溶液的pH________(填“增大”、“減小”或“不變”)。
(2)右上圖是一個太陽能路燈,圖中的④是蓄電池。鎳氫電池就是這樣一種與太陽能電池配套使用的蓄電池,白天用于充電,夜間供電。這種蓄電池容量大,充電放電循環壽命也較長。該蓄電池的總反應為Ni(OH)2 NiOOH+1/2H2↑。鎳氫電池的電解液采用30%的KOH溶液,白天充電反應時的陽極反應式為 ,夜間放電時,負極附近溶液的pH________(填“增大”、“減小”或“不變”)。
 II.X、Y、Z、Q、R5種短周期元素原子序數依次增大。化合物甲由X、Z、Q3種元素組成,常溫下,0.1mol·L-l甲溶液的pH =13。工業上常用電解QR飽和溶液生產甲
II.X、Y、Z、Q、R5種短周期元素原子序數依次增大。化合物甲由X、Z、Q3種元素組成,常溫下,0.1mol·L-l甲溶液的pH =13。工業上常用電解QR飽和溶液生產甲
(3)Q的原子結構示意圖為
(4)常溫下將R的單質通人甲溶液中,發生反應的離子方程式為
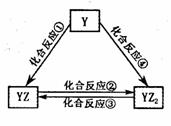
(5)若Y元素的單質能發生如右圖所示轉化,則Y元素是 。
已知:298K時,反應②生成1mol YZ2(g)時放出熱量283.O kJ·mol-1,
反應④生成1mol YZ2(g)時放出熱量393.5 kJ·mol-1,反應③的熱化學方程式為
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com