
X、Y、Z、U、V是元素周期表前四周期中的五種常見元素,其相關(guān)信息如下表:
|
元素 |
相關(guān)信息 |
|
X |
地殼中含量最多的金屬,其氧化物可用作耐火材料 |
|
Y |
單質(zhì)在常溫常壓下為黃綠色氣體 |
|
Z |
常溫常壓下,單質(zhì)是淡黃色固體,常在火山口附近沉積 |
|
U |
常溫下單質(zhì)遇濃硫酸鈍化,其一種核素的質(zhì)量數(shù)為56,中子數(shù)為30 |
|
V |
屬短周期元素,原子的最外層電子數(shù)是內(nèi)層電子數(shù)的2/5 |
請(qǐng)回答下列問(wèn)題:
(1)元素X位于周期表中第 周期第 族,其離子結(jié)構(gòu)示意圖為 。
(2)上述元素中最高價(jià)氧化物對(duì)應(yīng)的水化物酸性最強(qiáng)的是 (寫化學(xué)式),非金屬氣態(tài)氫化物還原性最強(qiáng)的是 (寫化學(xué)式)。
(3)在堿性條件下,Y的單質(zhì)可與UO2-反應(yīng)制備一種可用于凈水的鹽UO42-,該反應(yīng)的離子方程式是 。
(4)我國(guó)首創(chuàng)的海洋電池被大規(guī)模用于海洋燈塔。該電池是以X板為負(fù)極,鉑網(wǎng)為正極,海水為電解質(zhì)溶液,電池總反應(yīng)為:4X+3O2+6H2O=4X(OH)3。該電池正極反應(yīng)為 。
(5)已知25℃時(shí),Ksp[U(OH)3]=2.63×10-39,則該溫度下反應(yīng)U(OH)3+3H+ U3++3H2O的平衡常數(shù)K=
。
U3++3H2O的平衡常數(shù)K=
。
(16分)
(1)三、ⅢA  (3分,每空1分)
(3分,每空1分)
(2)HClO4 SiH4 (4分,每空2分)
(3)2FeO2-+ 3Cl2 + 8OH- = 2FeO42-+ 6Cl-+ 4H2O (3分)
(4)O2+4e-+2H2O=4OH-或3O2+12e-+6H2O=12OH- (3分)
(5)2.63×103 (3分,帶單位計(jì)算也給分)
【解析】
試題分析:(1)地殼中含量最多的金屬元素是鋁,則X是Al,鋁原子具有283的電子層結(jié)構(gòu),位于第三周期第IIIA族;1個(gè)氯原子失去3個(gè)電子變?yōu)殇X離子,則Al3+的核電荷數(shù)為13,具有28電子層結(jié)構(gòu);(2)氯氣在常溫常壓下是黃綠色氣體,則Y是氯元素,其最高價(jià)氧化物對(duì)應(yīng)水化物是高氯酸,HClO4是已知酸中酸性最強(qiáng)的酸;硫磺在常溫常壓下是淡黃色固體,則Z為硫元素;由于質(zhì)子數(shù)=質(zhì)量數(shù)—中子數(shù)=56—30=26,則U為鐵元素;短周期元素原子的內(nèi)層電子數(shù)可能是2或10,最外層電子數(shù)是內(nèi)層電子數(shù)的2/5,說(shuō)明電子層結(jié)構(gòu)為284,則V是硅元素;根據(jù)元素周期律可知,非金屬性:Si<S<Cl,則單質(zhì)的氧化性:Si<S<Cl2,氣態(tài)氫化物的還原性:SiH4>H2S>HCl;(3)Cl2是強(qiáng)氧化劑,能將FeO2-氧化為FeO42-,氯由0降為-1價(jià),鐵由+3價(jià)升為+6價(jià),根據(jù)化合價(jià)升降總數(shù)相等、電荷守恒、原子守恒可得:2FeO2-+ 3Cl2 + 8OH-= 2FeO42-+ 6Cl-+ 4H2O;(4)4Al+3O2+6H2O=4Al(OH)3,鋁由0升為+3價(jià),失去電子,發(fā)生氧化反應(yīng),說(shuō)明鋁作負(fù)極;氧由0降為—2價(jià),得到電子,發(fā)生還原反應(yīng),說(shuō)明氧氣是正極反應(yīng)物,根據(jù)電子、電荷、原子守恒可知,正極反應(yīng)式為O2+4e-+2H2O=4OH-或3O2+12e-+6H2O=12OH-;(5)25℃時(shí),Ksp[Fe(OH)3]=2.63×10-39,Kw=1.0×10-14,F(xiàn)e(OH)3+3H+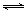 Fe3++3H2O,固體和純液體不能寫入平衡常數(shù)表達(dá)式,則該反應(yīng)的平衡常數(shù)K=c(Fe3+)/c3(H+)=[c(Fe3+)•c3(OH-)]/[c3(H+)•c3(OH-)]= Ksp[Fe(OH)3]/Kw3=2.63×10-39/(1.0×10-14) 3=2.63×103。
Fe3++3H2O,固體和純液體不能寫入平衡常數(shù)表達(dá)式,則該反應(yīng)的平衡常數(shù)K=c(Fe3+)/c3(H+)=[c(Fe3+)•c3(OH-)]/[c3(H+)•c3(OH-)]= Ksp[Fe(OH)3]/Kw3=2.63×10-39/(1.0×10-14) 3=2.63×103。
考點(diǎn):考查物質(zhì)結(jié)構(gòu)、元素周期律、氧化還原反應(yīng)方程式的配平、書寫正極反應(yīng)式、根據(jù)溶度積和水的離子積計(jì)算化學(xué)平衡常數(shù)等。


 名校名師培優(yōu)作業(yè)本加核心試卷系列答案
名校名師培優(yōu)作業(yè)本加核心試卷系列答案 全程金卷系列答案
全程金卷系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:


查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:


查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
 (2012?武漢模擬)[化學(xué)一選修 3:物質(zhì)結(jié)構(gòu)與性質(zhì)]有U、V、W、X、Y、Z 六種前四周期元素,原子序數(shù)依次增大,其相關(guān)信息如下表:
(2012?武漢模擬)[化學(xué)一選修 3:物質(zhì)結(jié)構(gòu)與性質(zhì)]有U、V、W、X、Y、Z 六種前四周期元素,原子序數(shù)依次增大,其相關(guān)信息如下表:| 元素編號(hào) | 相關(guān)信息比 |
| U | 所處的周期數(shù)、族序數(shù)分別與其原子序數(shù)相等 |
| V | 基態(tài)時(shí),電子分布在三個(gè)能級(jí)上,且各能級(jí)中電子數(shù)相等 |
| W | 基態(tài)時(shí),2p 軌道處于半充滿狀態(tài) |
| X | 與W元素處于同一周期,且X的第一電離能小于W的第一電離 |
| Y | 是第四周期元素中未成對(duì)電子數(shù)最多的元素 |
| Z | Z 的一種核素的質(zhì)量數(shù)為65,中子數(shù)為 36 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com