
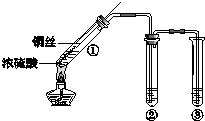
 某學校課外學習活動小組針對教材中銅與濃硫酸反應,提出了探究“能夠與銅反應的硫酸的最低濃度是多少?”的問題,并設計了如下方案進行實驗:
某學校課外學習活動小組針對教材中銅與濃硫酸反應,提出了探究“能夠與銅反應的硫酸的最低濃度是多少?”的問題,并設計了如下方案進行實驗:分析 (1)裝置是氣體發生裝置,需要在開始時檢查裝置的氣密性;
(2)二氧化硫是污染性氣體不能排放到空氣中,需要用氫氧化鈉溶液吸收,利用倒置的漏斗而不是將導氣管直接伸入燒杯中是防止液體倒吸;
(3)燒瓶中是銅和濃硫酸加熱反應生成硫酸銅、二氧化硫和水,裝置中長導氣管兼起導氣冷凝的作用,使水蒸氣冷凝回流;
(4)加入過氧化氫把亞硫酸鈉氧化為硫酸鈉,加入氯化鋇溶液反應生成硫酸鋇沉淀,通過過濾、洗滌、干燥得到沉淀稱量計算硫元素物質的量,依據硫元素守恒結合化學方程式計算需要反應的硫酸最低濃度.
解答 解:(1)實驗裝置是制備二氧化硫氣體的發生裝置,在實驗前需要檢驗裝置氣密性,防止裝置漏氣影響實驗,
故答案為:檢驗裝置氣密性;
(2)二氧化硫是污染性氣體不能排放到空氣中,需要用氫氧化鈉溶液吸收,利用倒置的漏斗而不是將導氣管直接伸入燒杯中是防止液體倒吸,
故答案為:SO2;防倒吸;
(3)燒瓶中是銅和濃硫酸加熱反應生成硫酸銅、二氧化硫和水,反應的化學方程式為:Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,裝置中長導氣管兼起導氣冷凝的作用,使水蒸氣冷凝回流,起到了確保硫酸溶液體積保持不變的作用;
故答案為:Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;長導管;
(4)加入過氧化氫把亞硫酸鈉氧化為硫酸鈉,加入氯化鋇溶液反應生成硫酸鋇沉淀,通過過濾、洗滌、干燥得到沉淀,稱量固體的質量為13.98g為硫酸鋇沉淀,物質的量=$\frac{13.98g}{233g/mol}$=0.06mol,依據硫元素守恒,被氧化的硫酸為0.06mol,依據化學方程式可知,Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,反應的硫酸物質的量為0.12mol,剩余硫酸物質的量=18mol/L×0.020L-0.12mol=0.24mol,剩余需要的最低濃度=$\frac{0.24mol}{0.02L}$=12mol/L,
故答案為:過濾、洗滌;干燥;12mol/L.
點評 本題考查了濃硫酸性質的分析應用,實驗設計方法的設計方法,掌握基礎是解題關鍵,題目難度中等.


 期末1卷素質教育評估卷系列答案
期末1卷素質教育評估卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 減小容器體積,平衡向右移動 | |
| B. | 加入催化劑,平衡不移動故正逆反應速率不變 | |
| C. | 增大c(X),X的轉化率增大 | |
| D. | 降低溫度,Y的轉化率增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溴離子具有氧化性 | B. | 氯氣是還原劑 | ||
| C. | 氯氣發生氧化反應 | D. | 氧化性:Cl2>Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不能發生丁達爾效應的分散系是溶液 | |
| B. | 將1 L 2 mol/L的FeCl3溶液制成膠體后,其中含有氫氧化鐵膠粒數為2NA | |
| C. | 納米粒子的大小與膠體粒子相當,但納米粒子的體系不一定是膠體 | |
| D. | 將飽和FeCl3溶液加熱至沸騰,制得Fe(OH)3膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某小組同學探究濃硫酸及其部分反應產物的化學性質,裝置如圖所示(夾持裝置略去).
某小組同學探究濃硫酸及其部分反應產物的化學性質,裝置如圖所示(夾持裝置略去).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某化學興趣小組的同學為探究二氧化硫的化學性質,設計了如圖所示的裝置.請回答下列問題.
某化學興趣小組的同學為探究二氧化硫的化學性質,設計了如圖所示的裝置.請回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 利用天然氣可制得以H2、CO等為主要組成的工業原料合成氣,反應為:CH4(g)+H2O(g)?CO(g)+3H2(g).
利用天然氣可制得以H2、CO等為主要組成的工業原料合成氣,反應為:CH4(g)+H2O(g)?CO(g)+3H2(g).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a1、a2均減小 | B. | a1減小,a2增大 | C. | a1、不變,a2增大 | D. | a1不變,a2減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com